Dióxido de enxofre
O dióxido de enxofre é um gás incolor, classificado como um óxido, emitido a partir da queima de combustíveis fósseis e um dos responsáveis pela chuva ácida.
Por Victor Ricardo Ferreira
PUBLICIDADE
O dióxido de enxofre é um gás muito utilizado em escala industrial. Ele é emitido de forma natural por atividades vulcânicas, mas também por atividades humanas nas indústrias e nos meios de transporte. Esse gás vem ganhando destaque devido aos seus impactos no meio ambiente e na saúde humana.
Fórmula
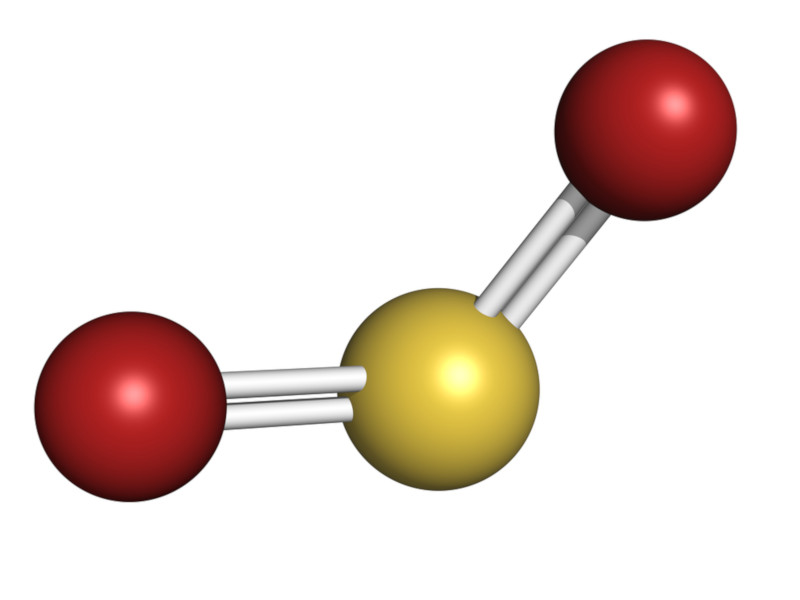
O dióxido de enxofre (SO2) é um gás incolor na temperatura ambiente, tóxico e sufocante. Também é um gás não inflamável e solúvel em água. Sua densidade é de 2,7 kg/m³ (cerca de 2 vezes mais denso que o ar atmosférico). Sua fórmula estrutural é composta por dois átomos de oxigênio e um átomo de enxofre ligados por ligações duplas covalentes em uma geometria angular.
.jpg)
Saiba mais: Alotropia do enxofre
Fontes emissoras
Parte do dióxido de enxofre disponível no ambiente é proveniente da decomposição de vegetação e de atividades vulcânicas, mas ainda pode vir da oxidação do sulfeto de hidrogênio pelo ar atmosférico como mostra a reação abaixo:
2 H2S (g) + 3 O2 (g) → 2 SO2 (g) + 2 H2O (g)
Outra fonte de emissão de dióxido de enxofre na atmosfera é a queima de materiais que contenham enxofre em sua formulação em indústrias e meios de transporte. A combustão de combustíveis fósseis, como o petróleo e o carvão, contribui com a liberação desse gás considerado um dos mais nocivos ao meio ambiente.

Os centros urbanos e centros industriais são uns dos principais responsáveis pela emissão de SO2 na atmosfera.
Aplicações
A aplicação mais importante do dióxido de enxofre é na escala industrial, na produção de ácido sulfúrico, mas também possui algumas utilizações secundárias, como gás de refrigeração em indústrias de bebidas e gelo; na fabricação de papel sulfite; na preservação de frutas secas, refrigerantes e vinhos, inibindo a atividade de leveduras.
Acesse também: Conheça melhor as características dos gases!
Efeitos sobre a saúde e o meio ambiente
Por se tratar de um gás com alta solubilidade em água, o SO2, liberado de forma natural ou a partir dos combustíveis fósseis, interage com as gotículas de água presentes na atmosfera, formando o ácido sulfuroso (H2SO3), conforme a reação a seguir:
2 SO2 (g) + 2 H2O (l) → H2SO3 (aq)
O gás sulfuroso, por sua vez, é oxidado, produzindo o ácido sulfúrico (H2SO4), um dos ácidos responsáveis pela chuva ácida. Essa chuva, devido ao pH reduzido, afeta diretamente as plantas, reduzindo a taxa de fotossíntese e atrapalhando seu crescimento.
Além disso, também aumenta a acidez do solo, rios e lagos, prejudicando a vida aquática, causando a morte de espécies. Em alguns casos, a chuva ácida também corrói a estrutura de monumentos e edificações.
Além do dano ambiental, que gera impactos diretamente aos seres humanos, o dióxido de enxofre é um gás tóxico que causa irritações no sistema respiratório, na pele e pode levar ao desenvolvimento de doenças cardiovasculares. Os principais sintomas aparentes ao ser exposto a esse gás é tosse, irritação nos olhos, náuseas, vômitos e dificuldades na respiração.





