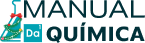Tabela periódica
Tabela periódica é a organização sistematizada das espécies atômicas de acordo com o seu número de prótons e suas características físico-químicas.
Por Laysa Bernardes Marques de Araújo
PUBLICIDADE
Para imprimir a tabela, clique aqui.
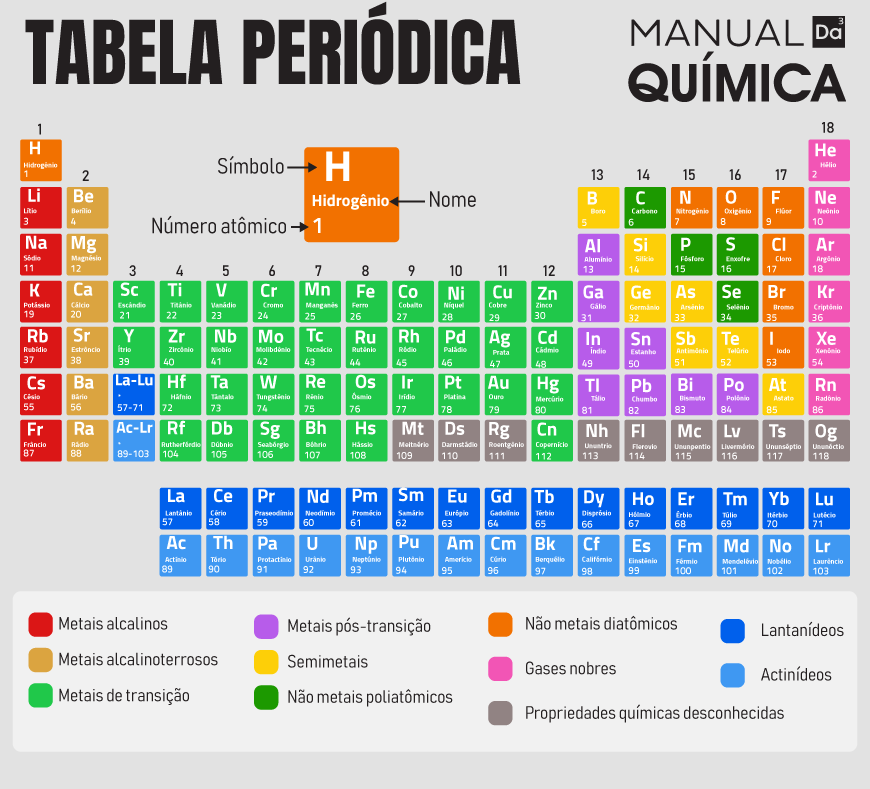
A tabela periódica é uma organização sistemática das espécies atômicas descobertas e onde é possível obter informações sobre elas, como número atômico e número de massa. Além disso, ela possibilita o estabelecimento de relações em torno das propriedades periódicas dos elementos, como raio atômico e eletronegatividade.
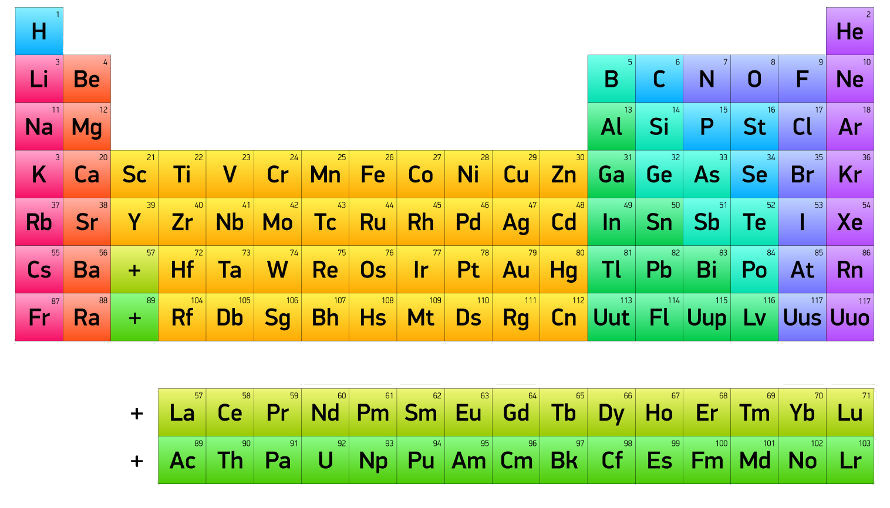
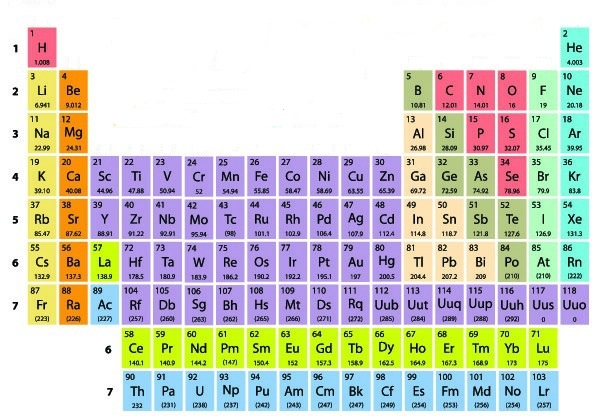
Criada por Dmitri Mendeleiev e atualizada por Julius Lothar Meyer, a versão atualizada contém 118 elementos posicionados em ordem crescente de número atômico. Ela é estruturada em grupos (colunas) e períodos (linhas). Cada grupo contém elementos com o mesmo número de elétrons na camada de valência, e os elementos de cada período possuem o mesmo número de camadas eletrônicas.
Leia também: Classificação dos elementos químicos na tabela periódica
Versão atual da tabela peródica
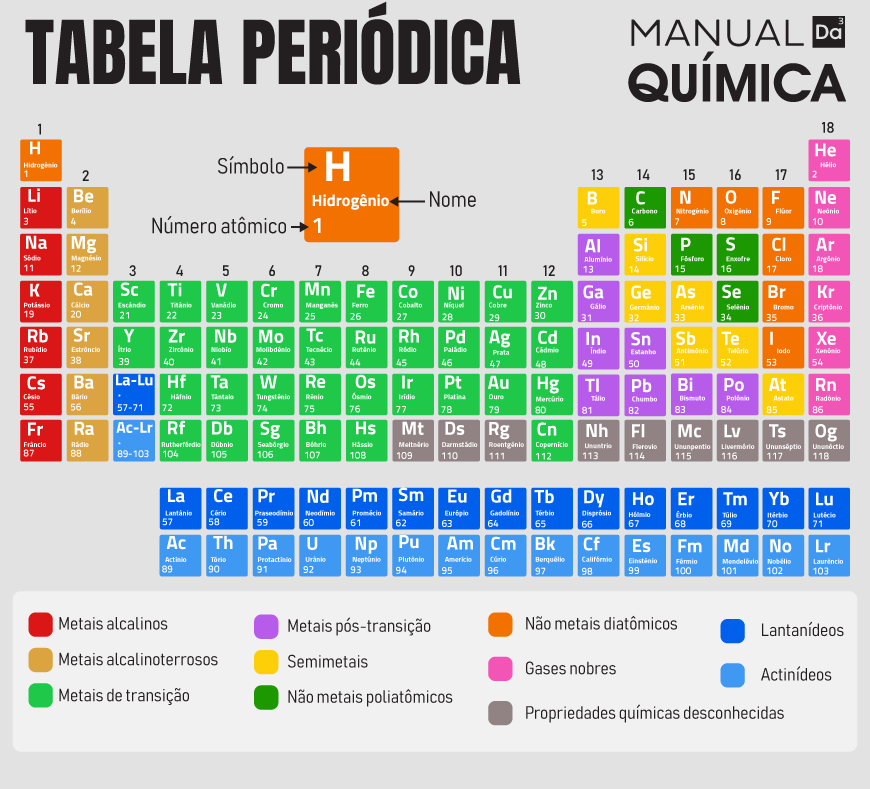
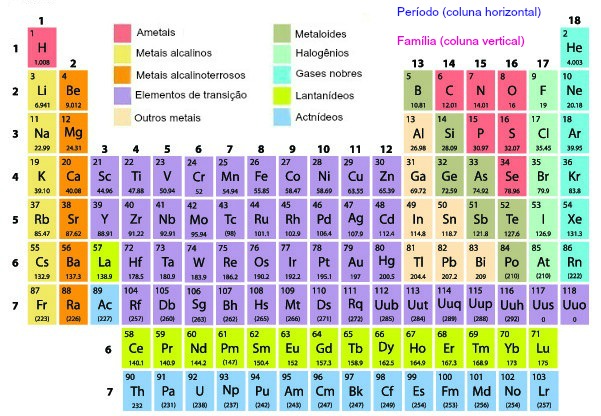
Organização da tabela periódica
→ Família ou grupos
As famílias ou grupos da tabela periódica são as colunas (classificadas de acordo com o número de elétrons na camada de valência), ou seja, cada grupo comporta elementos com o mesmo número de elétrons na camada de valência, consequentemente agrupa elementos com características físico-químicas em comum.
São ao total 18 grupos. Em alguns livros e artigos, pode-se encontrar a denominação família ou grupo com subdivisões do tipo A e B, mas essa denotação entrou em desuso por recomendação da União Internacional da Química Pura e Aplicada (Iupac). Atualmente a classificação é feita dividindo-se os elementos em colunas, chamadas de grupos, que vão do 1 ao 18.
-
Grupo 1 (metais alcalinos): hidrogênio (está posicionado no grupo 1, mas não possui semelhança com os demais elementos do grupo), lítio, sódio, potássio, rubídio, césio e frâncio.
-
Grupo 2 (metais alcalinoterrosos): berílio, magnésio, cálcio, estrôncio, bário e rádio.
-
Grupo 3: escândio, ítrio e série de lantanídeos (15 elementos) e actinídeos (15 elementos).
-
Grupo 4: titânio, zircônio, háfnio e rutherfórdio.
-
Grupo 5: vanádio, nióbio, tântalo e dúbnio.
-
Grupo 6: cromo, molibdênio, tungstênio e seabórgio.
-
Grupo 7: manganês, tecnécio, rênio e bóhrio.
-
Grupo 8: ferro, rutênio, ósmio, hássio.
-
Grupo 9: cobalto, ródio, irídio e meitnério.
-
Grupo 10: níquel, paládio e platina
-
Grupo 11: cobre, prata, ouro e roentgênio.
-
Grupo 12: zinco, cádmio, mercúrio e copernício.
-
Grupo 13: boro, alumínio, gálio, índio, tálio e nihônio.
-
Grupo 14: carbono, silício, germânio, estanho, chumbo e fleróvio.
-
Grupo 15: nitrogênio, fósforo, arsênio, antimônio, bismuto e moscóvio.
-
Grupo 16 (calcogênios): oxigênio, enxofre, selênio, telúrio, polônio e livermório.
-
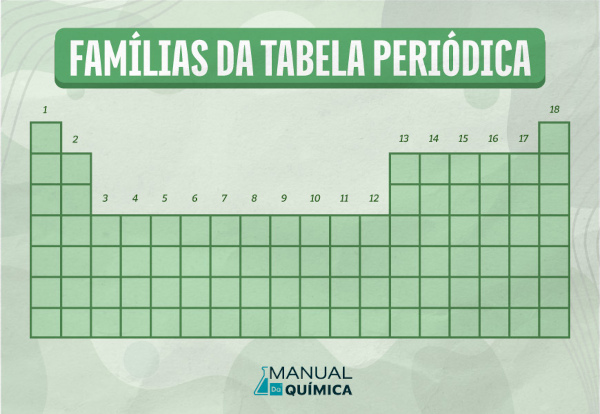
Grupo 17 (halogênios): flúor, cloro, bromo, iodo, astato e tenessino.
-
Grupo 18 (gases nobres): hélio, neônio, argônio, criptônio, xenônio, radônio e oganésson.
→ Períodos
Período é a classificação dada na horizontal, em linhas, ordenadas de acordo com o número de camadas eletrônicas. No primeiro período, por exemplo, estão os elementos que comportam seus elétrons em apenas uma camada. São sete períodos ao todo. Veja a seguir o número de elementos em cada um.
-
1º período: 2 elementos.
-
2º período: 8 elementos.
-
3º período: 8 elementos.
-
4º período: 18 elementos.
-
5º período: 18 elementos.
-
6º período: 32 elementos.
-
7º período: 32 elementos.
Veja também: Elementos de transição interna da tabela periódica
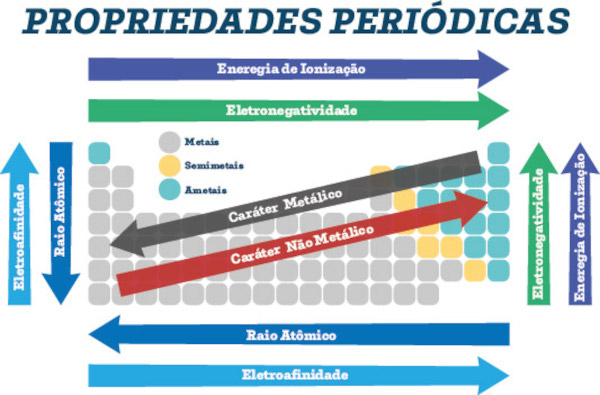
Propriedades periódicas
-
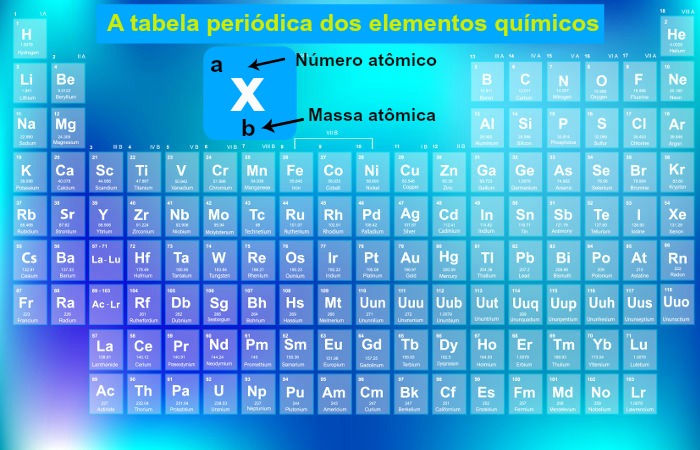
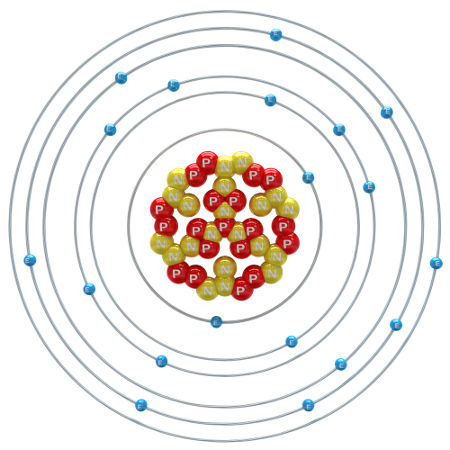
Configuração eletrônica: local de maior probabilidade de se encontrar os elétrons de um determinado átomo. Estando o átomo em estado neutro (sem carga), o número de elétrons será igual ao número de prótons, que é dado na tabela periódica. A informação sobre o número atômico fica disposta no lado superior esquerdo ao símbolo do elemento. A configuração eletrônica é feita a partir do número de elétrons de cada elemento e com o auxílio do diagrama de Linus Pauling, no qual os elétrons se organizam em camadas e subcamadas.
-
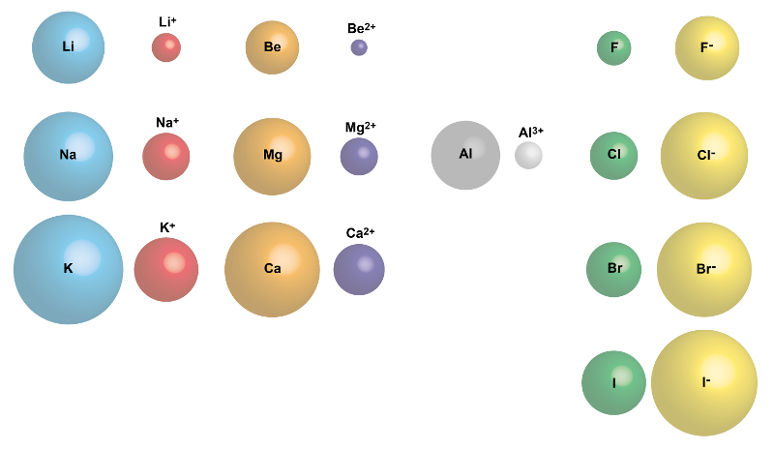
Raio atômico: varia conforme o número de elétrons que cada átomo comporta. Assim como na configuração eletrônica, o número de elétrons para átomos neutros é o mesmo que o número de prótons. O raio atômico é a distância entre o núcleo e o elétron da camada mais externa.
-
Eletronegatividade: é a predisposição que o átomo tem para atrair elétrons. Essa propriedade varia conforme a carga elétrica do átomo no estado fundamental e também pela proximidade da camada de valência com o núcleo do átomo.
-
Energia de ionização: é a energia necessária para a separação de um elétron do átomo. Conforme os elétrons vão sendo removidos, a energia de ionização vai aumentando. Essa energia varia conforme a distância do elétron a ser removido e o núcleo do átomo, pois o núcleo exerce atração e energia potencial elétrica, duas forças que dificultam a retirada do elétron.
-
Afinidade eletrônica ou eletroafinidade: é a energia liberada quando o átomo se adere a um elétron externo. Mede a força de atração que o átomo tem para capturar elétrons e se tornar um íon de carga negativa.
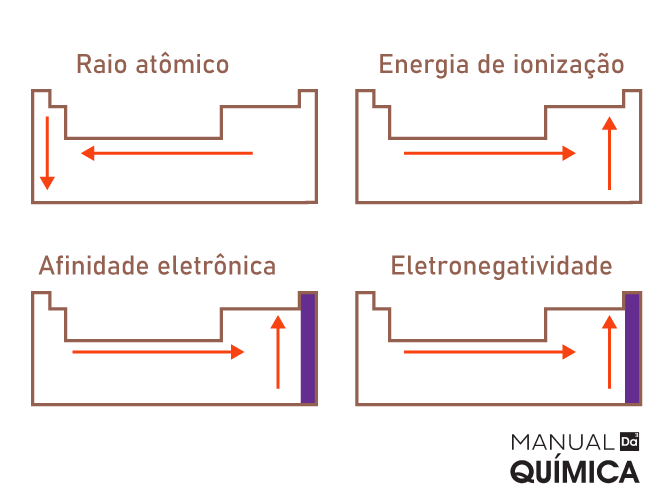
Para saber mais sobre essas propriedades, leia o nosso texto: propriedades periódicas.
Origem e história da tabela periódica
No intuito de organizar sistematicamente todos os elementos fundamentais da matéria, muitos cientistas propuseram tabelas que ordenavam os átomos das mais variadas formas, de acordo com características em comum ou por alguma propriedade específica. Em 1789, Antoine Lavoisier propôs uma lista com 33 elementos químicos, que foram organizados entre substâncias simples, metais, ametais e salificáveis ou terrosos. No entanto, a primeira tabela periódica aceita e a mais completa foi a proposta por Dmitri Mendeleiev em 1869.
Essa tabela se organizava de acordo com a massa atômica dos elementos e era composta, inclusive, por espaços para encaixar elementos que ainda não haviam sidos estudados ou reconhecidos, mas que poderiam ter suas propriedades previstas.
Com o passar do tempo, à luz de novas descobertas científicas, como a existência de prótons, nêutrons e novas espécies atômicas, tornou-se necessário reorganizar a tabela periódica. Foi Henry Moseley, em 1913, que reestruturou a tabela proposta por Mendeleiev, colocando os elementos em ordem crescente de número atômico. Atualmente são catalogados 118 espécies químicas, sendo 94 de ocorrência natural e 24 sintetizados em laboratório.
As últimas descobertas atômicas são espécies sintéticas. Trata-se dos elementos de número atômico 113, 115, 117 e 118, reconhecidos pela Iupac em dezembro de 2015.
Acesse também: Nomes dos novos elementos químicos
Curiosidades sobre a tabela periódica
-
Os elementos de número atômico 113, 115, 117 e 118, identificados e reconhecidos pela Iupac em 2015, foram batizados em 2016 como nihonium (Nh), moscovium (Mc), tennessine (Ts) e oganesson (Og), respectivamente.
-
Superpesados é o nome dado aos elementos químicos sintetizados recentemente em razão do alto número de prótons em relação às espécies atômicas de ocorrência natural.
-
Em 2017, a Organização das Nações Unidas (ONU) declarou que 2019 seria o Ano Internacional da Tabela Periódica, em mérito aos avanços científicos da Química, que propõe solução para questões que envolvem o bem-estar geral.
-
Em 1863, na tentativa de criar uma tabela para a organização dos átomos, o químico John Newlands usou um sistema de classificação inspirado nas oitavas musicais.
-
Mendeleiev publicou seu trabalho sobre a tabela periódica simultaneamente ao trabalho de Julius Lothar Meyer. Ambos sistematizaram a organização dos elementos atômicos de forma semelhante. O que levou Mendeleiev a ter mais notoriedade foram os espaços deixados, que previam a existência e as propriedades dos átomos que ainda seriam descobertos. Outro ponto foi a organização feita por Mendeleiev, que ignorou em alguns momentos a ordem da massa atômica, para se ter assim famílias químicas, compostas por elementos com propriedades em comum. Com isso, despretensiosamente, a tabela foi organizada também por ordem crescente de número atômico.
-
Dos 118 elementos catalogados na tabela periódica, 24 são artificiais, 94 são de ocorrência natural e, desses 94 elementos, 10 são produtos do decaimento radioativo.