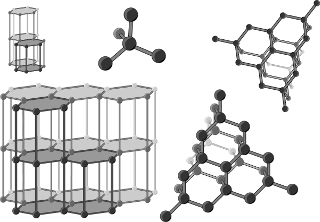
Alotropia do Fósforo
A alotropia do fósforo é um fenômeno responsável pela origem do fósforo branco e do fósforo vermelho.
Por Jennifer Rocha Vargas Fogaça

PUBLICIDADE
A alotropia ocorre quando um elemento químico é capaz de formar vários tipos de substâncias simples. O oxigênio, por exemplo, pode ligar-se e formar o gás oxigênio (O2) ou o gás ozônio (O3); o carbono pode ligar-se e formar o diamante ou a grafita; já o enxofre pode formar o enxofre rômbico ou o enxofre monoclínico.
Neste artigo falaremos mais especificadamente da alotropia do fósforo (P). Entre as formas alotrópicas do fósforo, as principais são o fósforo branco e o fósforo vermelho. Ambos são formados por ligações entre os átomos de fósforo que formam um tetraedro semelhante ao mostrado a seguir:
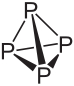
Molécula tetraédrica formada por átomos de fósforo
A diferença entre o fósforo branco e o vermelho está na quantidade de átomos. O fósforo branco é formado por moléculas com quatro átomos de fósforos ligados entre si (P4) na estrutura tetraédrica mencionada. Já o fósforo vermelho é constituído por macromoléculas formadas pela ligação dessas estruturas tetraédricas (P4), sendo representadas por Pn.
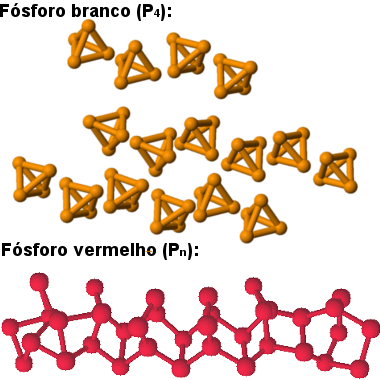
Estruturas das formas alotrópicas do fósforo
Essas quantidades de átomos diferentes resultam em propriedades físicas e químicas distintas. Veja algumas:
O fósforo branco é sólido em condições ambientes, tendo o aspecto parecido com o de uma cera. Além disso, ele é bastante reativo, tanto que precisa ser guardado em um frasco com água para não entrar em contato com o ar e sofrer combustão.

Fósforo branco guardado em recipiente com água*
Sua manipulação é perigosa, tendo em vista que pode causar queimaduras graves na pele e, se for ingerido, causar intoxicação grave. A ingestão de apenas 0,1 g de fósforo branco pode ser fatal.
O fósforo vermelho, por outro lado, possui coloração vermelha escura e é um pó amorfo.

Fósforo vermelho em pó
Ele é bem menos reativo que o fósforo branco, mas pode entrar em combustão quando friccionado. Ao contrário do que a maioria das pessoas acredita, o fósforo vermelho não se encontra na cabeça do palito. Inicialmente era assim, mas os riscos de acidentes eram grandes, tendo em vista que os palitos dentro da caixa podiam friccionar-se uns com os outros e todos queimarem. Muitos guardavam as caixinhas de fósforos nos bolsos e assim podiam sofrer queimaduras.
Por essa razão, atualmente o fósforo costuma vir na parte lateral da caixinha de fósforo. Alguns países colocam o fósforo na cabeça do palito na forma de P4S3, por isso é possível também acender o palito friccionando-o em alguma superfície.

No Brasil e em muitos países, o fósforo vermelho encontra-se na parte áspera da superfície da caixa, e não na cabeça do palito
* Direitos autorais da imagem: W. Oelen / Wikimedia Commons.
Aproveite para conferir a nossa videoaula relacionada ao assunto: