Isomeria plana de cadeia
Na isomeria plana de cadeia, os compostos isômeros apresentam cadeias carbônicas diferentes.
Por Diogo Lopes Dias

PUBLICIDADE
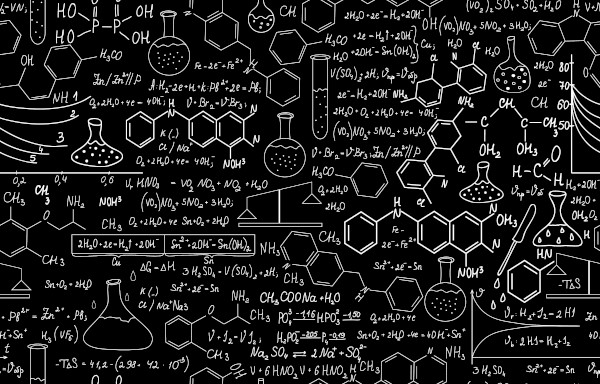
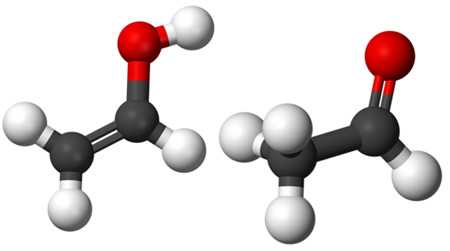
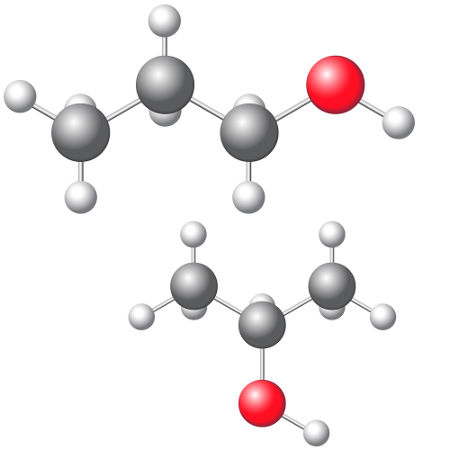
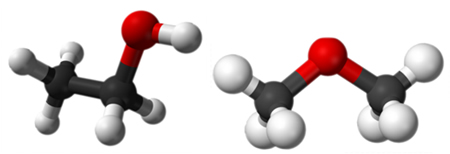
A isomeria plana de cadeia é um dos cinco tipos de isomeria plana existentes. Para que sejam isômeros, os compostos devem apresentar a mesma fórmula molecular, isto é, os mesmos tipos e quantidades de átomos que formam as substâncias. No exemplo a seguir, temos duas fórmulas estruturais diferentes, mas ambas apresentam a mesma fórmula molecular:
![]()
O tipo de isomeria plana é determinado pelas diferenças entre as fórmulas estruturais dos compostos. No caso da isomeria plana de cadeia, a diferença está no tipo de cadeia de cada uma das substâncias. Por esse motivo, é interessante relembrar as classificações que as cadeias podem receber:
-
Aberta: Aquela que apresenta extremidades livres (carbonos nas extremidades);
![]()
-
Fechada: Aquela que não possui extremidades livres. Os carbonos ligam-se de modo que a cadeia forme um ciclo;
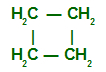
-
Normal: Cadeia que não apresenta mais de duas extremidades livres ou, no caso de cadeia fechada, não apresenta carbono fora do ciclo;
![]()
-
Ramificada: Cadeia que apresenta três ou mais extremidades livres. No caso das fechadas, elas são ramificadas quando apresenta um ou mais carbonos fora do ciclo;
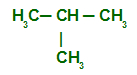
-
Saturada: Cadeia que, entre os carbonos, há apenas ligações do tipo simples;
![]()
-
Insaturada: Cadeia que, entre os carbonos, há pelo menos uma ligação dupla ou tripla.
Não pare agora... Tem mais depois da publicidade ;)
![]()
-
Homogênea: Cadeia que não apresenta heteroátomo, isto é, Nitrogênio (N), Oxigênio, Fósforo (P) ou Enxofre (S), entre os átomos de carbono.
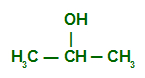
-
Heterogênea: Cadeia que apresenta pelo menos um heteroátomo, isto é, os elementos Nitrogênio (N), Oxigênio, Fósforo (P) ou Enxofre (S), entre os átomos de carbono.
![]()
Depois dessa explanação sobre as classificações das cadeias, podemos determinar se, entre substâncias, existe ou não isomeria plana de cadeia. Para tal, vamos utilizar os três exemplos a seguir:
— Butano e Isobutano
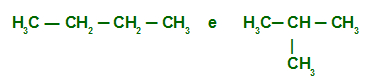
Podemos observar que tanto o isobutano quanto o butano apresentam fórmula molecular C4H10, logo, são isômeros. O butano apresenta cadeia aberta normal, e o isobutano apresenta cadeia aberta ramificada. Portanto, trata-se de isômeros de cadeia.
— Dimetilamina e Etilamina
![]()
Podemos observar que tanto a dimetilamina (à esquerda) quanto a etilamina (à direita) apresentam fórmula molecular C2H7N; logo, são isômeros. A dimetilamina apresenta cadeia aberta heterogênea, e a etilamina apresenta cadeia aberta homogênea. Portanto, trata-se de isômeros de cadeia.
— Ciclopentano e 3-metil-but-1-eno
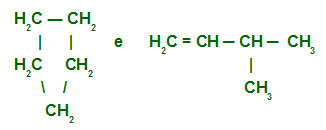
Podemos observar que tanto o ciclopentano quanto o 3-metil-but-1-eno apresentam fórmula molecular C5H10; logo, são isômeros. O ciclopentano apresenta cadeia fechada, e o 3-metil-but-1-eno apresenta cadeia aberta. Portanto, trata-se de isômeros de cadeia.
Por Me. Diogo Lopes Dias