Monóxido de carbono
Por Victor Ricardo Ferreira

PUBLICIDADE
O monóxido de carbono é um gás emitido por ações humanas ou naturais, produto da reação incompleta de combustão de substâncias ricas em carbono que causa severos danos à saúde dos seres vivos, por ser extremamente tóxico.
Aspectos gerais
O monóxido de carbono é um gás à temperatura ambiente, de aparência incolor, sem cheiro e sem sabor. É caracterizado como um asfixiante químico, pois impede a utilização biológica do oxigênio e, por isso, é extremamente tóxico. Por conta de suas características físicas, é um gás de difícil detecção pelos sentidos humanos, o que o torna ainda mais perigoso.
Leia também: Características gerais dos gases
Na escala industrial, o monóxido de carbono é utilizado na produção de metais, como ferro e níquel, retirando o oxigênio por oxirredução de seus respectivos minerais. Ele também é utilizado na produção de substâncias orgânicas como ácido acético, metanol, plásticos etc.
O monóxido de carbono também foi utilizado durante a Segunda Guerra Mundial nos campos de concentração, mais especificamente nas câmaras de gás.
Propriedades
Apresenta fórmula química CO e é classificado, dentro das funções inorgânicas, como óxido. Seu ponto de fusão é de - 205,07 °C e seu ponto de ebulição é de -191,55 °C, sua densidade é igual a 1,25 kg/m3.
Quanto à solubilidade, é parcialmente solúvel em água, sendo melhor solubilizado em clorofórmio, ácido acético, etanol e outros solventes orgânicos. É um gás inflamável e tóxico até em baixas concentrações.
Como é produzido

O monóxido de carbono é um dos produtos formados na combustão incompleta de compostos que possuem carbono em sua fórmula. Quando ocorre a queima desses compostos (geralmente combustíveis como gasolina, querosene e diesel) com quantidade insuficiente de gás oxigênio, a reação não se processa como é esperado de uma queima total, que libera dióxido de carbono. Outros produtos, como o monóxido de carbono e o carbono sólido (fuligem), são formados nessas condições.
Esse tipo de reação ocorre, em maior proporção, nas indústrias e nos automóveis, mas também está presente em queimadas, fornos e fogões a lenha, equipamentos de aquecimento de água e de residências que funcionam à base de gás ou querosene.
Leia também: Petróleo
Como acontece a intoxicação
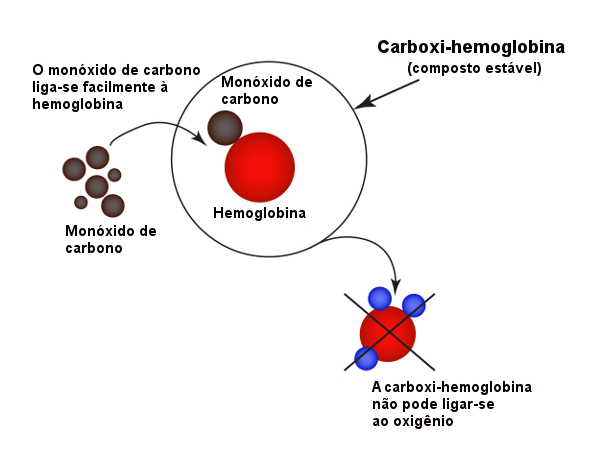
A intoxicação por monóxido de carbono dá-se por meio das vias respiratórias, pelas quais o gás vai para os pulmões e entra na corrente sanguínea. Após a difusão do monóxido pelas veias, esse se liga à hemoglobina (que é a proteína contida no sangue responsável pelo transporte de oxigênio para os tecidos do corpo) e entra em competição com o próprio O2.
Devido ao fato de o monóxido possuir uma afinidade cerca de 250 vezes maior com a hemoglobina do que o gás oxigênio, ele forma com ela a carboxihemoglobina, impedindo a formação da oxi-hemoglobina (oxigênio ligado à hemoglobina). Com isso, o fornecimento de oxigênio para o corpo fica prejudicado, causando asfixia.
Efeitos após inalação de monóxido de carbono
Os efeitos da inalação dependem da concentração em que se encontra o gás e do tempo de exposição a ele. Em baixas concentrações, o monóxido de carbono pode causar dores de cabeça, fraqueza, tonturas e náuseas. A inalação de gás em altas concentrações agrava os sintomas, podendo causar desmaios, fortes dores de cabeça, diminuição da frequência cardíaca, respiração lenta, convulsões e morte.
Por ser um gás inodoro e incolor, a exposição a grandes quantidades de monóxido de carbono pode levar a uma rápida perda de consciência, sem sinais aparentes e sem as chances de aviso ou detecção.



