Estados físicos da matéria
Os estados físicos fundamentais da matéria são sólido, líquido e gasoso, que se diferenciam pelo menor ou maior grau de agregação entre suas partículas.
Por Jennifer Rocha Vargas Fogaça
PUBLICIDADE
O tema “estados físicos” é amplamente conhecido, e a maioria, senão todos, dos alunos que começa seus estudos em Química sabe que os três estados físicos básicos da matéria são sólido, líquido e gasoso. Porém, vale a pena recordar o que caracteriza esses três estados, pois, em Química, estuda-se a matéria, as transformações sofridas por ela, bem como a energia envolvida nessas transformações; sendo que as propriedades da matéria, como a densidade, estão intimamente ligadas com o seu estado físico. Além disso, as transformações da matéria podem envolver mudanças de estados físicos, que incluem também trocas de energia.
A matéria pode ser definida de maneira bem simplificada como sendo tudo aquilo que tem massa e volume e ocupa um lugar no espaço. Portanto, a matéria é constituída de minúsculas partículas, que podem ser átomos, moléculas, íons e assim por diante. De modo que, simplificadamente, o que diferencia um estado físico de outro é a organização dessas partículas, se elas estão mais próximas umas às outras ou mais afastadas, isto é, se estão mais agregadas ou menos agregadas. Por isso, os estados físicos podem ser corretamente chamados de “estados de agregação”.
Veja as principais diferenças entre os estados físicos:
* Sólido: Nesse estado, as partículas estão bem próximas umas às outras, de modo que não se movimentam. Estão bem organizadas e, por isso, possuem forma e volume fixos, não podendo sofrer compressão. O gelo é um bom exemplo disso.
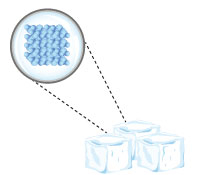
Cubos de gelo – estado sólido
* Líquido: Nesse estado, as partículas possuem maior liberdade de movimentação que no estado sólido, pois estão um pouco mais afastadas umas das outras, havendo certo espaço entre elas. Por essa razão, as substâncias líquidas, como a água, possuem forma variável, adaptando-se ao recipiente em que estão contidas, mas não podem ser comprimidas, pois possuem volume constante.
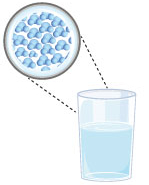
Copo com água – estado líquido
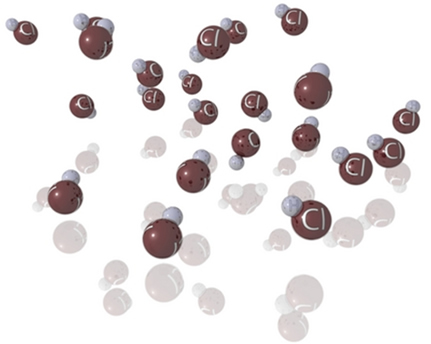
* Gasoso: Nesse estado, as partículas estão bem afastadas umas das outras, possuindo grande liberdade de movimentação. Por isso, os gases e os vapores, como o vapor de água, não possuem forma nem volume fixos, conformando-se de acordo com o recipiente e podendo ser comprimidos.
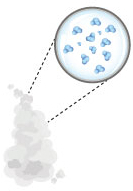
Estado gasoso
Assim, quando uma substância recebe ou perde energia na forma de calor, ela muda de estado físico. Com isso, ela continua sendo a mesma substância, mas mudou somente a organização de suas partículas constituintes. Dependendo do tipo de interação entre essas partículas, isto é, dependendo da intensidade das forças intermoleculares, a quantidade de energia necessária para provocar a mudança de estado físico varia. Se a força intermolecular for bem intensa, precisará de mais energia, ou seja, precisaremos aquecer bastante a substância para mudá-la de estado físico e vice-versa.
Existe ainda um quarto estado da matéria que não é muito estudado porque quase não é encontrado aqui na Terra, que é o plasma. Este, por sua vez, é um conjunto quente e denso de átomos livres, elétrons e íons, com distribuição quase neutra e comportamento coletivo. Para formar esse estado, é necessário que a matéria no estado gasoso seja aquecida a temperaturas elevadíssimas, como ocorre, por exemplo, no núcleo das estrelas, como o do nosso Sol, em que existem certas regiões de sua superfície que estão em aproximadamente 84.000ºC.
Por Jennifer Fogaça
Graduada em Química
Aproveite para conferir nossas videoaulas sobre o assunto: