Reações com óxidos ácidos
Reações com óxidos ácidos são processos químicos em que podemos ter a produção de diferentes tipos de substâncias, tais como sais, ácidos e água.
Por Diogo Lopes Dias

PUBLICIDADE
Reações com óxidos ácidos são fenômenos químicos que ocorrem quando substâncias dessa classe de óxidos são colocadas em um mesmo recipiente com substâncias químicas capazes de interagir com elas, como:
-
Água;
-
Óxidos básicos;
-
Óxidos anfóteros.
Quando uma reação entre um óxido ácido e uma dessas substâncias ocorre, há sempre a formação de um ou mais produtos, o que vai depender exclusivamente dos materiais colocados para reagir com o óxido.
Reação entre óxidos ácidos e água
Sempre que um óxido ácido é colocado para reagir com água, ocorre a formação de um ácido inorgânico.
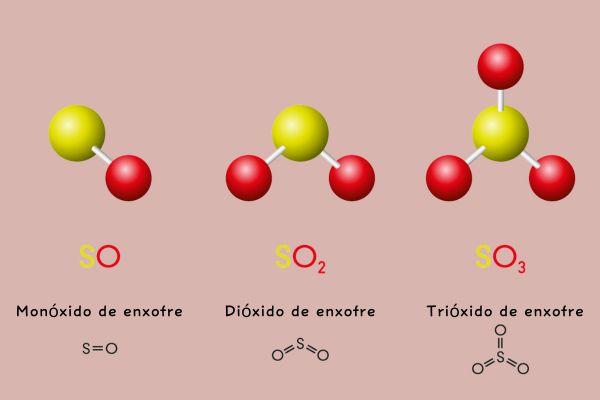
Exemplo: Reação entre o dióxido de enxofre e água
SO2 + H2O → H2SO3
Reação entre óxidos ácidos e bases inorgânicas
Sempre que um ácido interage com uma base inorgânica, há a formação de um sal e água, da seguinte forma:
-
Água: Formada pela interação entre os hidrogênios da hidroxila (OH) da base e o oxigênio do óxido;
-
Sal: É formado pela interação entre o metal da base, que é o cátion do sal, e um ânion, resultante da interação entre o óxido e a água.
Exemplo: Reação entre o trióxido de enxofre (SO3) e o hidróxido de cálcio [Ca(OH)2]
SO3 + Ca(OH)2 →
-
1º Como envolve a reação entre um óxido ácido e uma base, há a formação de água e um sal (X):
SO3 + Ca(OH)2 → H2O + X
Para saber qual é o sal formado, devemos inicialmente saber qual é o ácido formado por esse óxido em presença de água:
SO3 + H2O → H2SO4
Esse ácido apresenta o ânion sulfato (SO4-2).
-
2º No sal formado, há a interação entre o cátion da base, que é o cálcio (Ca+2), e o ânion (SO4-2), resultante da formação do ácido formado acima (H2SO4), o que resulta no sal sulfato de cálcio (CaSO4). A seguir, veja a equação completa e balanceada desse processo:
SO3 + Ca(OH)2 → H2O + CaSO4
Reação entre óxidos ácidos e óxidos básicos
Sempre que um óxido ácido é colocado para reagir com um óxido básico, ocorre a formação de apenas um sal (Y), que é formado pela interação entre o metal do óxido básico, que é o cátion do sal, e um ânion, resultante da interação entre o óxido e a água.
Exemplo: Reação entre o dióxido de carbono (CO2) e o óxido de sódio
-
1º Como envolve a reação entre um óxido ácido e um óxido básico, há a formação de um sal (Y):
CO2 + NaOH → Y
Para saber qual é o sal formado, devemos inicialmente saber qual é o ácido formado por esse óxido em presença de água:
CO2 + H2O → H2CO3
Esse ácido apresenta o ânion carbonato (CO3-2).
-
2º No sal formado, acontece a interação entre o cátion da base, que é o sódio (Na+1), e o ânion (CO3-2), resultante da formação do ácido acima (H2CO3), o que resulta no sal carbonato de sódio (Na2CO3). Observe a equação completa e balanceada desse processo:
CO2 + Na2O → Na2CO3
Reação entre óxidos ácidos e óxidos anfóteros
Sempre que um óxido ácido interage com um óxido anfótero, este age como se fosse um óxido básico. Logo, nesse tipo de reação, há a formação de um sal inorgânico. Esse sal é formado pela interação entre o metal da base, que é o cátion do sal, e um ânion, resultante da interação entre o óxido e a água.
Exemplo: Reação entre o trióxido de cromo VI (CrO3) e o óxido de alumínio (Al2O3)
-
1º Como envolve a reação entre um óxido ácido e um óxido anfótero, que atua como um óxido básico, há a formação de um sal (Z):
CrO3 + Al2O3 → Z
Para saber qual é o sal formado, devemos inicialmente saber qual é o ácido formado por esse óxido em presença de água:
CrO3 + H2O → H2CrO4
Esse ácido apresenta o ânion crômico (CrO4-2).
-
2º No sal formado, há a interação entre o cátion do óxido básico, que é o alumínio (Al+3), e o ânion (CrO4-2), resultante da formação do ácido acima (H2CrO4), o que resulta no sal dicromato de alumínio [Al2(CrO4)3]. Veja a seguir a equação completa e balanceada desse processo:
3 CrO3 + 1 Al2O3 → Al2(CrO4)3