Alcanos
Os alcanos são hidrocarbonetos saturados de cadeia aberta. Segundo as regras da IUPAC para nomenclatura dos compostos, o nome dos alcanos termina em “-ano”.
Por Stéfano Araújo Novais

PUBLICIDADE
Alcanos são hidrocarbonetos que apresentam apenas ligações simples entre os átomos de carbono, o que significa que são saturados. Além disso, possuem cadeia aberta e fórmula geral igual a CnH2n+2. Como consequência dessa definição, todos os átomos de carbono nos alcanos possuem hibridização sp³. No sistema oficial de nomenclatura da IUPAC, alcanos tem o nome terminado em “-ano”.
Alcanos apresentam densidade menor que da água, além de serem hidrofóbicos. É por isso que o petróleo, rico em alcanos, flutua na água em situações de vazamento. Os pontos de fusão e ebulição dos alcanos varia de acordo com o volume molecular, ou seja, quanto maior a cadeia, maiores serão esses valores. São aplicados na confecção de combustíveis, mas também em insumos petroquímicos e como solventes.
Leia também: O que são alcenos?
Resumo sobre alcanos
- Alcanos são hidrocarbonetos de cadeia aberta e saturada.
- Todo alcano possui fórmula geral do tipo CnH2n+2.
- Os alcanos são menos densos que a água, além de serem também hidrofóbicos.
- Quanto maior a cadeia do alcano, maiores seus valores de fusão e ebulição.
- Na natureza, os alcanos possuem duas fontes importantes: o gás natural e o petróleo.
- Os alcanos são importantes na indústria petroquímica, além de serem usados como combustíveis e solventes.
O que são alcanos?
Alcanos são hidrocarbonetos que apresentam apenas ligações simples entre átomos de carbonos. Como são hidrocarbonetos, possuem apenas carbono e hidrogênios na sua composição.
Característica dos alcanos
Os alcanos, sendo uma classe de hidrocarboneto, possuem apenas carbono e hidrogênio em sua constituição. Apresentam apenas ligações simples entre átomos de carbono e, dessa forma, todas as ligações entre esses elementos são do tipo sigma (σ), com os átomos de carbono adotando uma geometria tetraédrica (hibridização sp3).
Outro ponto importante é que os alcanos são saturados, uma vez que as ligações C–C não podem reagir para que haja adição de hidrogênios à molécula. Sua fórmula geral é CnH2n+2, isso quer dizer que para cada átomo de carbono há o dobro mais 2 átomos de hidrogênio.
Veja também: Como saber a eletronegatividade de um elemento?
Propriedades dos alcanos
Os alcanos são compostos considerados apolares, uma vez que a eletronegatividade dos átomos de carbono e hidrogênio são similares. Com isso, podemos afirmar que as interações intermoleculares que imperam nos alcanos são as do tipo dipolo induzido-dipolo induzido (forças de dispersão de London).
Elas são consequência da mobilidade eletrônica dentro das moléculas de alcano, o que permite a formação de dipolos temporários, as quais induzem a formação de dipolos em moléculas de alcanos adjacentes e assim se criando a interação.
Tais interações são as mais fracas dentre as conhecidas, contudo, são somativas, o que quer dizer que, quanto maior a molécula, maior a superfície de interação e, dessa forma, mais intensas são as forças de London. Isso causa um impacto direto na evolução dos pontos de ebulição dos alcanos. Percebe-se que, para alcanos de cadeia normal, as temperaturas de ebulição aumentam com o aumento da cadeia de alcano, conforme é mostrado na tabela a seguir.
|
Alcano |
Temperatura de ebulição (°C) |
|
CH4 |
-161,7 |
|
CH3CH3 |
-88,6 |
|
CH3CH2CH3 |
-42,1 |
|
CH3CH2CH2CH3 |
-0,5 |
|
CH3CH2CH2CH2CH3 |
36,1 |
|
CH3CH2CH2CH2CH2CH3 |
68,7 |
|
CH3CH2CH2CH2CH2CH2CH3 |
98,4 |
|
CH3CH2CH2CH2CH2CH2CH2CH3 |
125,6 |
A influência do volume molecular na intensidade das forças de London é nítida quando se avaliam as temperaturas de ebulição de alcanos isômeros. Pegando-se três alcanos de fórmula C5H12, podemos pensar no pentano (cinco carbonos em linha, cadeia normal), 2-metilbutano (com uma ramificação) e no 2,2-dimetilpropano (com duas ramificações).
O maior número de ramificações faz com que o volume molecular diminua, tornando as interações dipolo induzido-dipolo induzido menos intensas, fazendo com que a temperatura de ebulição seja também menor.
|
Temperaturas de ebulição de alcanos de fórmula C5H12 (em °C) |
||
|
pentano |
2-metilbutano |
2,2-dimetilpropano |
|
36,1 |
27,9 |
9,5 |
Em termos de temperaturas de fusão, os alcanos apresentam, com algumas exceções, um aumento dos valores com o aumento do volume molecular, porém com uma regularidade menor quando comparada à evolução dos valores de temperaturas de ebulição.
Quando falamos de fusão (passagem do estado sólido para o líquido), também devemos levar em consideração o empacotamento da estrutura cristalina, ou seja, os níveis de proximidade e compactação das moléculas no estado sólido. Quanto mais empacotadas, obviamente, maior a energia necessária para o afastamento molecular e, consequentemente, maior a temperatura de fusão.
É aí que surge um comportamento interessante. Quando se é avaliada a progressão dos pontos de fusão dos alcanos de cadeia normal, percebe-se um padrão de alternância e evolução curta, mas, quando se separam os alcanos com número par de átomos de carbonos dos alcanos com número ímpar de átomos de carbono, vemos um padrão de crescimento mais regular e de fácil percepção.
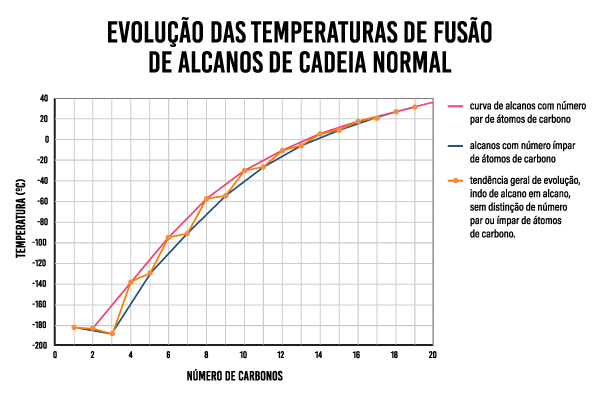
O motivo? Alcanos com número ímpar de átomos de carbono formam estruturas cristalinas menos compactadas se comparadas aos alcanos de número par. Por isso, quando se comparam as curvas de evolução de temperaturas de fusão, a dos alcanos de número par fica acima.
Em termos de solubilidade, os alcanos, como sendo compostos apolares, acabam sendo solúveis apenas em compostos apolares, e insolúveis em compostos polares (como a água). Portanto, podemos dizer que os alcanos são hidrofóbicos (ou lipofílicos).
Considerando a sua densidade (massa específica), os alcanos são os menos densos de todos os grupos de compostos orgânicos. Percebe-se um aumento da densidade com o aumento da massa molecular, mas todos com valores abaixo de 1,0 g/mL (densidade máxima da água, a 4 °C).
|
Densidade de alcanos de cadeia normal |
|
|
Número de carbonos |
Densidade (g/mL, 20 °C) |
|
5 |
0,56 |
|
6 |
0,66 |
|
7 |
0,68 |
|
8 |
0,70 |
|
9 |
0,72 |
|
10 |
0,73 |
|
11 |
0,74 |
|
12 |
0,75 |
|
13 |
0,75 |
|
20 |
0,79 |
|
30 |
0,81 |
Por isso, percebemos que o petróleo, que é uma mistura de hidrocarbonetos rica em alcanos, flutua na água.

Nomenclatura dos alcanos
Os alcanos são hidrocarbonetos, o que implica que, segundo as regras de nomenclatura oficial da IUPAC, terão o sufixo “–o”. Porém, sendo cadeias saturadas, o infixo de todo alcano é “–an–”. Portanto, podemos complementar que todo alcano, independentemente de ser normal ou ramificado, terminará seu nome em “–ano”.
Vejamos alguns exemplos de alcanos sendo nomeados de acordo com as regras da IUPAC:
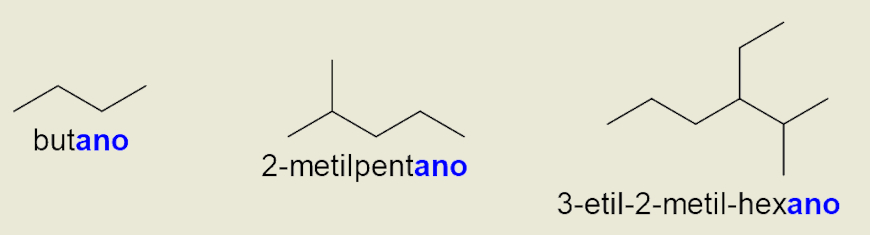
Para que serve um alcano?
Na natureza, os alcanos possuem duas fontes importantes: o gás natural e o petróleo. Sendo assim, são amplamente empregados no setor de energia, além de serem a base de toda indústria petroquímica.

Alcanos não são importantes só na produção de combustíveis, sejam eles sólidos, líquidos e gasosos, mas também na fabricação de lubrificantes, ceras parafínicas, além de serem os constituintes majoritários do asfalto.

A indústria química também se aproveita alcanos para serem utilizados como solventes apolares, altamente lipofílicos, como é o caso do hexano.
Alcanos, alcenos e alcinos
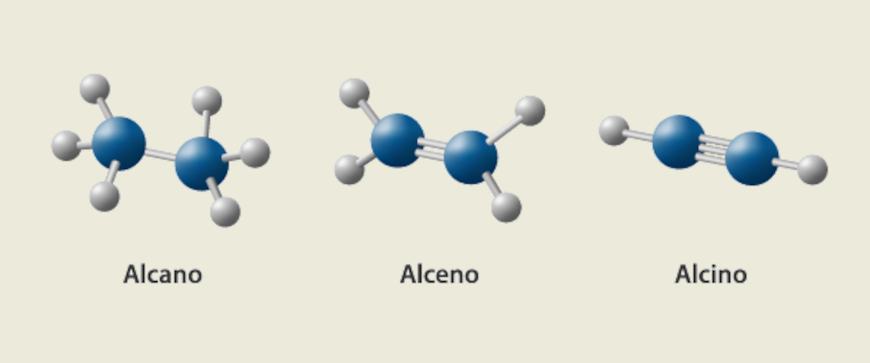
Alcanos, alcenos e alcinos são classes de hidrocarbonetos, mas com diferenças que, embora sejam simples, são muito significativas. Os alcanos, como já discorrido anteriormente, são hidrocarbonetos de cadeia aberta e saturada, ou seja, contendo apenas ligações simples entre os átomos de carbono.
Já os alcenos e alcinos são também hidrocarbonetos de cadeia aberta, porém insaturada. Os alcenos possuem uma ligação dupla entre átomos de carbono, enquanto os alcinos possuem uma ligação tripla entre os átomos de carbono. Em termos de nomenclatura, podem ser distinguidos pelo infixo. Assim, enquanto alcanos possuem o infixo “–an–“, os alcenos possuem o infixo “–en–“ e os alcinos, por sua vez, possuem o infixo “–in–“.
Saiba mais: Regras da IUPAC — nomenclatura dos compostos orgânicos
Exercícios resolvidos sobre alcanos
Questão 1. (FCMS-JF – Medicina/2025.1) Os hidrocarbonetos são compostos orgânicos formados apenas por átomos de carbono e hidrogênio e podem ser classificados de acordo com o tamanho da cadeia carbônica e o número de ramificações. Considere os seguintes hidrocarbonetos:
Butano (C4H10), isobutano (C4H10), Hexano (C6H14) e 2-metilpentano (C6H14).
Considerando a influência da estrutura (tamanho da cadeia e ramificações) sobre o ponto de ebulição, podemos afirmar que a ordem correta do ponto de ebulição dos hidrocarbonetos listados, do mais baixo para o mais alto será?
A) Isobutano < Butano < 2-Metilpentano < Hexano.
B) Butano < Isobutano < Hexano < 2-Metilpentano.
C) Hexano < 2-Metilpentano < Butano < Isobutano.
D) 2-Metilpentano < Butano < Isobutano < Hexano.
Resposta: Letra A.
O ponto de ebulição dos alcanos é dependente do seu volume molecular, ou seja, quanto maior o tamanho da molécula, mais intensas são as interações dipolo induzido-dipolo induzido, mais altas, portanto, serão as temperaturas de ebulição. Por isso, a ordem crescente de pontos de ebulição é igual à ordem crescente de volume molecular.
Primeiramente, há dois compostos com 4 carbonos, que terão ponto de ebulição menor que os dois compostos com 6 carbonos. No caso, o isobutano é uma forma ramificada (metilpropano), portanto tem menor volume e, consequentemente, menor ponto de ebulição que o butano, de cadeia normal.
Depois, a mesma análise se faz entre os dois compostos com seis carbonos: o 2-metilpentano possui um volume molecular menor que o hexano e, dessa forma, o hexano possui um maior ponto de ebulição.
Questão 2. (UNICENTRO/2020) Por ser relativamente simples, sensível e efetiva para separar os componentes de misturas, a cromatografia gasosa é uma das ferramentas muito utilizadas na química. Nessa técnica, os componentes, na forma de vapor, são gradualmente separados com base na sua volubilidade: do mais volátil para o menos volátil. É amplamente usada em análises quantitativas e qualitativas de espécies químicas e para determinar constantes termoquímicas, tais como calores de solução e vaporização, pressão de vapor e coeficientes de atividade. (POR SER, 2019).
Com base nessas informações, numa mistura de hidrocarbonetos contendo pentano, hexano, etano, propano e butano, o primeiro componente a ser separado é o
A) pentano.
B) hexano.
C) etano.
D) propano.
E) butano.
Resposta: Letra C.
Como a ordem de separação é de acordo com a volatilidade, será separado primeiro aquele de menor ponto de ebulição. Entre os alcanos, possuirá menor ponto de ebulição aquele que tiver menor volume molecular que, nesse caso, é o etano, pois conta com apenas dois átomos de carbono.
Fontes
BRUICE, P. Y. Organic Chemistry. 8. ed. Upper Saddle River, Nova Jersey: Pearson Education Inc., 2015.
HAYNES, W. M. (ed.) CRC Handbook of Chemistry and Physics. 95a ed. CRC Press: 2014.
MULLER, P. Glossary of terms used in physical organic chemistry (IUPAC Recommendations 1994). Pure and Applied Chemistry, v. 66, n. 5, p. 1086, 1994.
SOLOMONS, T. W. G.; FRYHLE, C. B.; SNYDER, S. A. Química Orgânica: volume 2. 12. ed. Rio de Janeiro: LTC, 2018.