Alcenos
Os alcenos são hidrocarbonetos de cadeia aberta que apresentam uma ligação dupla entre átomos de carbono. Recebem o sufixo -o e o infixo -en- na nomenclatura oficial.
Por Stéfano Araújo Novais

PUBLICIDADE
Alcenos são hidrocarbonetos de cadeia aberta que apresentam uma ligação dupla entre átomos de carbono. São também chamados de alquenos ou olefinas. Os alcenos possuem fórmula geral CnH2n, apresentando propriedades físicas muito semelhantes às dos demais hidrocarbonetos de cadeia aberta (alcanos e alcinos). São suscetíveis a ataques eletrofílicos, além de serem oxidados em meio ácido ou básico.
Os alcenos, como hidrocarbonetos, apresentam o sufixo -o, mas, por conta da insaturação, apresentam o infixo -en- na sua nomenclatura oficial. Dentre os alcenos existentes, os que possuem mais destaque na indústria são o eteno e o propeno, que são precursores químicos de moléculas mais complexas e também monômeros para polímeros como o polietileno e o polipropileno.
Leia também: O que são alcanos?
Resumo sobre alcenos
- Alcenos são hidrocarbonetos de cadeia aberta que possuem uma ligação dupla entre os átomos de carbono.
- A fórmula geral dos alcenos é do tipo CnH2n.
- Os alcenos são suscetíveis às reações de adição eletrofílica e oxidação.
- Segundo a nomenclatura oficial, os alcenos recebem o sufixo -o dos hidrocarbonetos, e o infixo -en- para indicar a insaturação.
- O eteno e o propeno são os alcenos de maior aplicabilidade industrial.
O que são alcenos?
Alcenos são hidrocarbonetos de cadeia aberta que apresentam uma ligação dupla entre dois átomos de carbono. Outra forma de se referir a esses compostos é como alquenos ou olefinas.
Características dos alcenos
Os alcenos, por serem hidrocarbonetos, apresentam apenas átomos de carbono e hidrogênio na sua constituição. Possuem cadeia aberta, insaturada (por conta da ligação dupla entre carbonos), mas podem ser ramificados. São sempre homogêneos, uma vez que nos hidrocarbonetos não há possibilidade de presença de heteroátomos. A fórmula geral dos alcenos é CnH2n. Isso significa que, para cada átomo de carbono presente (n), existe o dobro de átomos de hidrogênio (2n).
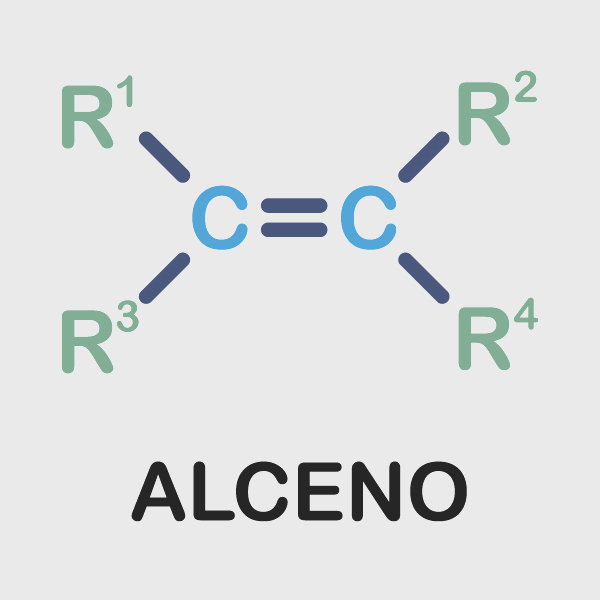
Em termos de propriedades físicas, os alcenos são muito semelhantes aos demais hidrocarbonetos de cadeia aberta (alcanos e alcinos) de tamanho semelhante. Assim sendo, os alcenos de até quatro átomos de carbono são gases à temperatura ambiente e muito pouco polares. Contudo, os alcenos são ligeiramente mais solúveis em água (um solvente polar) que os alcanos, uma vez que o carbono sp2 confere uma maior eletronegatividade dada à densidade eletrônica da ligação pi. A densidade dos alcenos é menor que a da água.
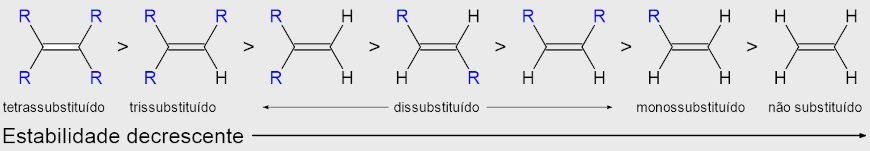
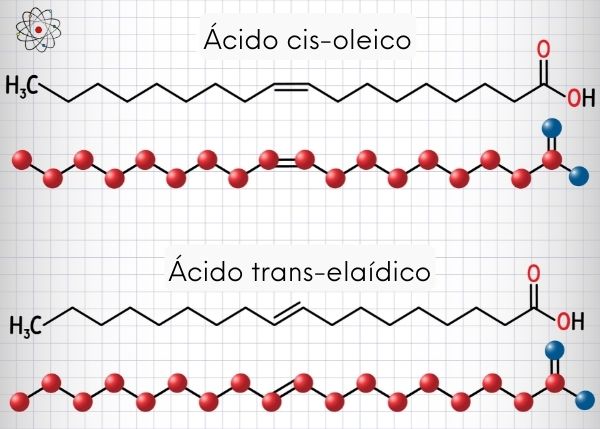
No caso dos alcenos dissubstituídos, a forma cis (com os dois radicais, um em cada carbono sp2, para o mesmo lado) é menos estável que a forma trans (com os dois radicais, um em cada carbono sp2, para lados opostos), pois ter os dois radicais para o mesmo lado da ligação dupla cria um congestionamento de nuvens eletrônicas, o que aumenta a repulsão.
Em termos de propriedades químicas, os alcenos (como os alcinos, mas não como os alcanos) são propícios a sofrerem reações de adição eletrofílica. A ligação pi, como anteriormente dito, apresenta uma maior densidade eletrônica, o que permite a reação com um eletrófilo. Além disso, outro ponto que auxilia nas reações de adição é o fato da ligação pi ser mais fraca que a ligação sigma, sendo esta facilmente quebrada.
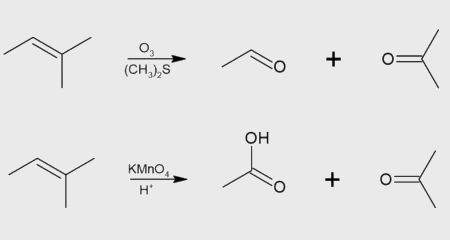
Os alcenos podem também ser oxidados, tanto em meio ácido quanto em meio básico, por diversos agentes oxidantes, como o permanganato de potássio (KMnO4) ou ozônio (O3). No caso de uma oxidação em meio básico (oxidação branda), apenas a ligação pi é quebrada, gerando a formação de um diol vicinal:
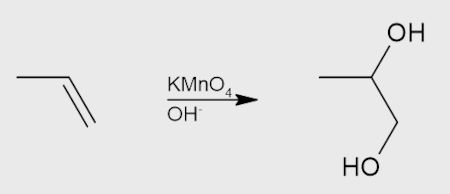
Já no caso da oxidação com ozônio (ozonólise) ou em meio ácido (oxidação enérgica), tanto a ligação pi quanto a ligação sigma são rompidas, dando origem a produtos carbonilados: no caso da ozonólise, aldeídos (se o carbono sp2 não for ramificado) ou cetonas; no caso da oxidação enérgica, ácidos carboxílicos (se o carbono sp2 não for ramificado) ou cetonas.
Nomenclatura dos alcenos
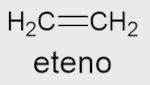
Segundo as normas da IUPAC (União Internacional de Química Pura e Aplicada), os hidrocarbonetos recebem o sufixo -o. Contudo, os alcenos, possuidores de uma ligação dupla entre dois átomos de carbono, devem apresentar o infixo -en-, para indicar a presença da insaturação. Como há a obrigação de existir a ligação dupla para ser um alceno, não existe o alceno com apenas um único carbono.
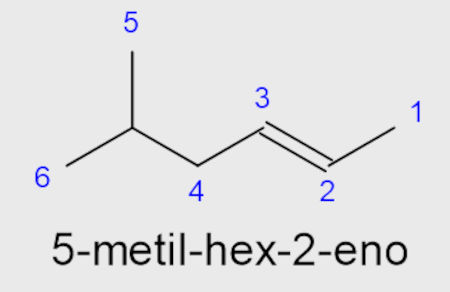
A insaturação deve ter sua posição indicada para alcenos de cadeia aberta com mais de três carbonos, uma vez que mais de uma posição é possível. Havendo uma ramificação no alceno, a insaturação possui prioridade e, dessa forma, a numeração deve iniciar na extremidade mais próxima à ligação dupla, de modo que esta fique no carbono de menor posição.
Veja este exemplo:
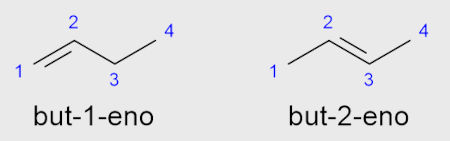
Para alcenos com mais de três carbonos, como o but-1-eno e but-2-eno, a ligação dupla pode aparecer em mais de uma posição possível. Sendo assim, deve-se indicar a sua posição no nome oficial, anteriormente ao infixo.
Diferenças entre alcenos, alcinos e alcanos
As diferenças entre alcanos, alcenos e alcinos se iniciam, basicamente, na estrutura. Embora todos sejam hidrocarbonetos de cadeia aberta, os alcanos são de cadeia saturada (todos os carbonos são sp3), enquanto alcenos e alcinos são insaturados.
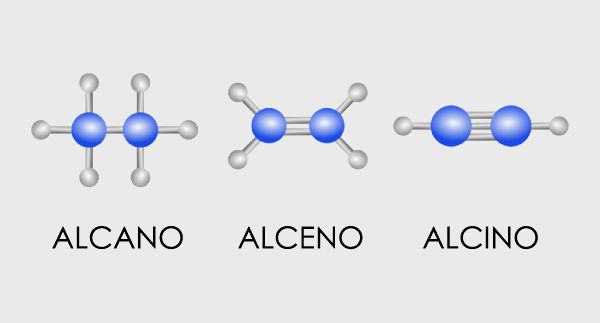
Contudo, como mostra a imagem acima, a insaturação de alcenos se dá por meio de ligações duplas entre átomos de carbono (carbonos sp2), já nos alcinos, por meio de ligações triplas entre átomos de carbono (carbonos sp).
Os alcenos e alcinos, como dito anteriormente, são um pouco mais eletronegativos que os alcanos, graças à maior densidade eletrônica trazida pela ligação pi. Com isso, alcenos e alcinos são ligeiramente mais solúveis em água do que alcanos. Alcanos, não possuindo ligações pi, não sofrem reações de adição eletrofílica, diferentemente de alcenos e alcinos. Alcanos, na verdade, são mais propensos às reações de substituição.
Outra diferença também está na fórmula geral desses compostos:
|
Alcanos |
CnH2n+2 |
|
Alcenos |
CnH2n |
|
Alcinos |
CnH2n-2 |
Aplicações dos alcenos
O eteno (C2H4) é um dos alcenos mais importantes. Não só utilizado no processo de maturação de frutas, esse simples alceno é também muito importante para a síntese de diversos outros produtos químicos, como:
- etanol, um álcool combustível e também utilizado como solvente e precursor sintético de outras moléculas;
- ácido acético, usado na fabricação de polímeros de vinilacetato, do solvente etilacetato e de polímeros de celulose acetato;
- etilenoglicol, um produto utilizado como anticongelante;
- dicloroeteno, usado na fabricação do cloreto de vinila (precursor do PVC), além de servir como solvente;
- polietileno, um dos mais importantes polímeros plásticos da indústria.

O propeno (C3H6) também apresenta grande importância na indústria química, como na preparação de:
- álcool isopropílico, um importante solvente, utilizado na síntese da propanona;
- cumeno (isopropilbenzeno), usado na preparação industrial do fenol e da propanona;
- óxido de propileno, que é usado na fabricação de poliésteres e poliuretano;
- polipropileno, outro importante polímero plástico da indústria.
Saiba mais: Polímeros — o que são, para que servem e do que são feitos?
Exercícios resolvidos sobre alcenos
Questão 1. (UNESC/2025.1) O etileno (C2H4) é um hormônio natural de amadurecimento que acelera o processo de maturação em diversas frutas, como banana, tomate e abacate. Ele estimula a produção de enzimas que degradam o amido em açúcar, tornando as frutas mais doces e com melhor sabor. Sabe-se que as propriedades químicas do etileno, assim como de muitos compostos orgânicos, são influenciadas pela hibridização dos átomos de carbono.
Qual é a hibridização dos átomos de carbono do etileno?
- sp.
- sp2.
- sp3.
- dsp3.
- d2sp3.
Resposta: Letra B.
O etileno (ou eteno), é um alceno de apenas dois carbonos, em que ambos apresentam a ligação dupla. Por terem uma ligação dupla e duas ligações simples, tais carbonos apresentam hibridização sp2.
Questão 2. (UECE – 2ª Fase – 2º dia/2025.2) O composto 3-etil-4-metilpent-2-eno é um hidrocarboneto insaturado que apresenta ramificações em sua cadeia principal. Com base na nomenclatura da IUPAC, assinale a alternativa que apresenta corretamente a fórmula molecular correspondente a esse composto.
- C8H14.
- C7H12.
- C7H14.
- C8H16.
Resposta: Letra D.
Os alcenos possuem fórmula geral CnH2n, ou seja, para cada átomo de carbono, há o dobro de átomos de hidrogênio. O 3-etil-4-metilpent-2-eno é um composto com 8 átomos de carbono: 5 da cadeia principal, mais 2 do radical etil, mais 1 do radical metil. Portanto, se há 8 átomos de carbono, por conseguinte, há 16 átomos de hidrogênio, por isso a fórmula C8H16.
Fontes
BRUICE, P. Y. Organic Chemistry. 8. ed. Upper Saddle River, Nova Jersey: Pearson Education Inc., 2015.
INTERNATIONAL UNION OF PURE AND APPLIED CHEMISTRY. Nomenclature of organic chemistry: IUPAC recommendations and preferred names 2013. Prepared by Henri A. Favre and Warren H. Powell. Cambridge, UK: Royal Society of Chemistry, 2014. E-book. Atualizado por G. P. Moss. Disponível em: https://iupac.qmul.ac.uk/BlueBook/PDF/BlueBookV3.pdf. Acesso em: 31 mar. 2026.
MULLER, P. Glossary of terms used in physical organic chemistry (IUPAC Recommendations 1994). Pure and Applied Chemistry, v. 66, n. 5, p. 1086, 1994.
SOLOMONS, T. W. G.; FRYHLE, C. B.; SNYDER, S. A. Química Orgânica: volume 2. 12. ed. Rio de Janeiro: LTC, 2018.
WADE, L. G. Structure and synthesis of alkenes: uses and sources of alkenes. In: WADE, L. G. Organic Chemistry. [S. l.]: LibreTexts, 2022. Disponível em: https://chem.libretexts.org/Courses/Nassau_Community_College/Organic_Chemistry_I_and_II/07%3A_Structure_and_Synthesis_of_Alkenes