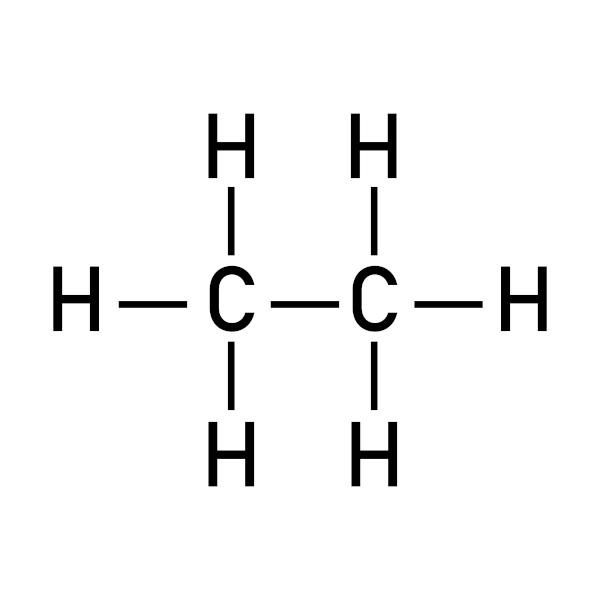
Reações de substituição em alcanos
Reações de substituição em alcanos são processos orgânicos que envolvem reagentes como halogênios, ácidos inorgânicos e que resultam em diferentes compostos orgânicos.
Por Diogo Lopes Dias
PUBLICIDADE
As reações de substituição de alcanos são processos químicos em que esses hidrocarbonetos são colocados para reagir com compostos inorgânicos específicos, e, durante a ocorrência desse processo, as substâncias trocam átomos entre si, originando outras.
Os compostos químicos que podem ser formados em uma reação de substituição em alcanos dependem do composto inorgânico utilizado. Com relação a esse aspecto, listamos a seguir os tipos de substituições, os reagentes utilizados e os produtos formados nesse tipo de reação.
-
Halogenação: utiliza cloro, bromo ou iodo e forma haleto orgânico e hidrácido inorgânico (o hidrácido é um ácido que não apresenta oxigênio em sua composição);
-
Nitração: utiliza ácido nítrico e forma nitrocomposto e água;
-
Sulfonação: utiliza ácido sulfúrico e forma ácido sulfônico e água.
É importantíssimo ressaltar que, sempre que uma reação de substituição em alcanos é realizada, uma ligação sigma deve ser rompida na molécula desse composto entre um carbono e um hidrogênio, como na molécula de etano:
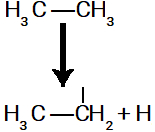
Quebra da ligação sigma no etano
No etano, as moléculas apresentam o mesmo número de hidrogênios e carbonos, e o mesmo NOX, logo são iguais. Porém, caso o alcano apresente carbonos com quantidades de hidrogênios diferentes, ocorrerá o rompimento da sigma entre ele e o hidrogênio, em moléculas diferentes, como no pentano:
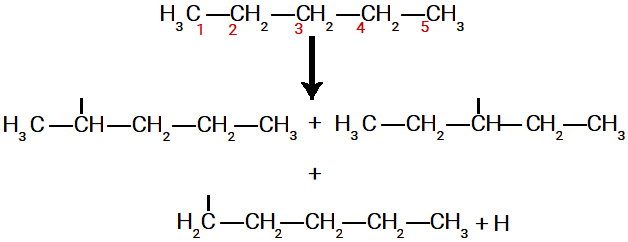
Quebra das ligações sigma no pentano
O pentano apresenta os carbonos 1 e 2 com NOX e número de hidrogênios diferentes, e o carbono 3 apresenta o mesmo NOX e número de hidrogênios que o carbono 2, porém com ligantes completamente diferentes (ele está ligado a dois grupos metil). Portanto, esse alcano seria capaz de formar três substâncias orgânicas diferentes em uma reação de substituição.
Quando mais de um composto orgânico é formado, o principal deles, formado em maior quantidade, é aquele que apresenta o maior caráter eletrônico, o que pode ser facilmente identificado pela ordem decrescente de prioridade:
Carbono terciário > carbono secundário > carbono primário
Reações por halogenação
É o tipo de reação de substituição em alcanos em que esses compostos, ao reagir com um halogênio molecular (cloro-Cl2, bromo-Br2, iodo-I2), formam haleto orgânico e ácido inorgânico.
Como vimos anteriormente, ocorre o rompimento de uma ligação sigma no alcano entre um carbono e um hidrogênio, fazendo com que surja um sítio de ligação na cadeia carbônica, além do hidrogênio, que fica livre no meio.
.jpg)
Rompimento da ligação sigma no alcano
Ao mesmo tempo, acontece a quebra da ligação sigma existente no halogênio molecular, fazendo com que cada um dos átomos fique livre no meio:

Rompimento da ligação sigma no halogênio molecular
Por fim, um dos átomos do halogênio deve ligar-se ao átomo de hidrogênio, formando um hidrácido inorgânico; e o outro átomo do halogênio liga-se ao sítio de ligação na cadeia carbônica, formando o haleto orgânico.
Exemplo: Halogenação por bromo do propano
-
1ª ocorrência: quebra da ligação sigma entre um carbono e um hidrogênio da cadeia.
Como os carbonos de número 1 e 2 apresentam características diferentes (NOX e número de hidrogênios) em uma molécula do propano, a sigma é rompida no carbono 1 e em outra molécula no carbono 2.
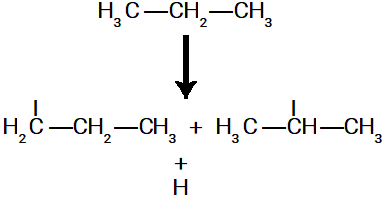
Exemplo do rompimento de ligações sigma no propano
-
2ª ocorrência: quebra da ligação sigma entre os átomos de bromo.

Quebra da ligação sigma entre os átomos de bromo
-
3ª ocorrência: ligação de um átomo de bromo no sítio criado em cada uma das moléculas.
Como existem dois tipos de moléculas, com sítios de ligação criados em diferentes carbonos, são formados dois diferentes de haletos orgânicos.
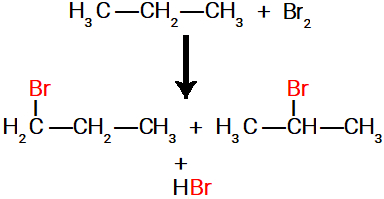
Possíveis haletos orgânicos formados na bromação do propano
Reações por nitração
É o tipo de reação de substituição em alcanos em que esses compostos, ao reagir com o ácido nítrico (HNO3), formam nitrocomposto e água.
Como vimos anteriormente, rompe-se no alcano uma ligação sigma entre um carbono e um hidrogênio, fazendo com que surja um sítio de ligação na cadeia carbônica, além do hidrogênio, que fica livre no meio.
.jpg)
Rompimento da ligação sigma no alcano
Ao mesmo tempo, ocorre a quebra da ligação sigma existente entre o nitrogênio e o grupo hidroxila (OH) no ácido nítrico, fazendo com que fiquem livres no meio o hidróxido (OH-) e o grupo NO2:
.jpg)
Rompimento da ligação sigma no ácido nítrico
Por fim, um o grupo OH liga-se ao átomo de hidrogênio, formando água, e o grupo NO2 liga-se ao sítio de ligação na cadeia carbônica, formando o nitrocomposto.
Exemplo: Nitração do butano
-
1ª ocorrência: quebra da ligação sigma entre um carbono e um hidrogênio da cadeia.
Como os carbonos de número 1 e 2 apresentam características diferentes (NOX e número de hidrogênios) em uma molécula do butano, a sigma é rompida no carbono 1 e em outra molécula no carbono 2.
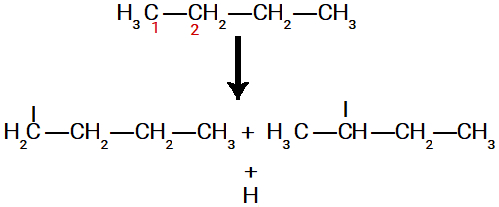
Exemplo do rompimento de ligações sigma no butano
-
2ª ocorrência: quebra da ligação sigma no ácido nítrico.
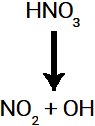
Rompimento da ligação sigma no ácido nítrico
-
3ª ocorrência: ligação de um grupo NO2 no sítio criado em cada uma das moléculas.
Como existem dois tipos de moléculas, com sítios de ligação criados em diferentes carbonos, são formados dois diferentes nitrocompostos.
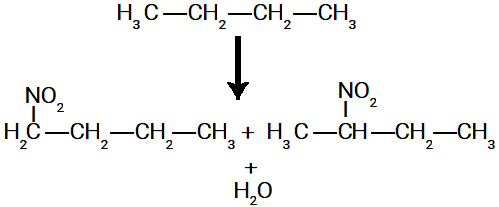
Possíveis nitrocompostos formados na nitração do butano
Reações por sulfonação
É o tipo de reação de substituição em alcanos em que esses compostos, ao reagir com o ácido sulfúrico (H2SO4), formam ácidos sulfônicos e água.
Como vimos anteriormente, no alcano, ocorre o rompimento de uma ligação sigma entre um carbono e um hidrogênio, fazendo com que surja um sítio de ligação na cadeia carbônica, além do hidrogênio, que fica livre no meio.
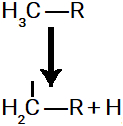
Rompimento da ligação sigma no alcano
Ao mesmo tempo, ocorre a quebra da ligação sigma existente entre o enxofre e o grupo hidroxila (OH) no ácido nítrico, fazendo com que fiquem livres no meio o hidróxido (OH-) e o grupo SO3H:
.jpg)
Rompimento da ligação sigma no ácido sulfúrico
Por fim, um o grupo OH deve ligar-se ao átomo de hidrogênio, formando água, e o grupo SO3H liga-se ao sítio de ligação na cadeia carbônica, formando o ácido sulfônico.
Exemplo: Sulfonação do metil-propano
-
1ª ocorrência: quebra da ligação sigma entre um carbono e um hidrogênio da cadeia.
Como os carbonos de número 1 e 2 apresentam características diferentes (NOX e número de hidrogênios) em uma molécula do metil-propano, a sigma é rompida no carbono 1 e em outra molécula no carbono 2.
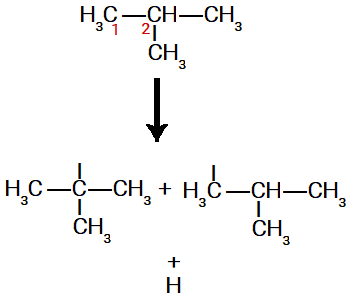
Exemplo do rompimento de ligações sigma no metil-propano
-
2ª ocorrência: quebra da ligação sigma no ácido sulfúrico.
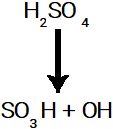
Rompimento da ligação sigma no ácido sulfúrico
-
3ª ocorrência: ligação de um grupo SO3H no sítio criado em cada uma das moléculas.
Como existem dois tipos de moléculas, com sítios de ligação criados em diferentes carbonos, são formados dois diferentes ácidos sulfônicos.
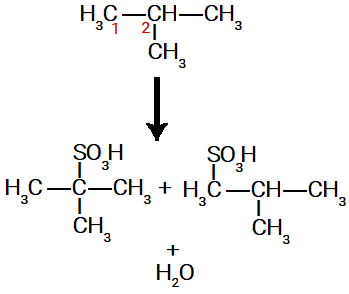
Possíveis ácidos sulfônicos formados na sulfonação do metil-propano