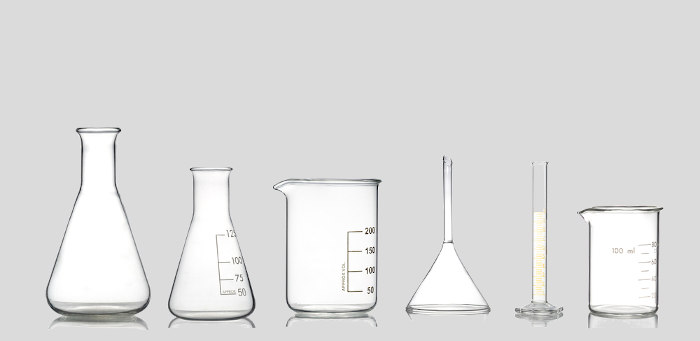
Experimento para determinar o teor de álcool na gasolina
Propomos neste texto um procedimento prático para determinar o teor de álcool (etanol) na gasolina.
Por Diogo Lopes Dias

PUBLICIDADE
Neste texto propomos um experimento prático para determinar a quantidade de álcool (etanol) presente em qualquer tipo de gasolina. Acompanhe o passo a passo e algumas informações relevantes:
a) Aspecto legal (Legislação)
De acordo com a resolução do Conselho Interministerial do Açúcar e do Álcool (Cima), o teor de álcool permitido na gasolina é de 27%. Caso a quantidade de álcool não esteja dentro desse patamar, temos um combustível adulterado, o que pode trazer danos mecânicos ao veículo com o tempo.
b) Materiais necessários para o experimento
-
1 Béquer de 100 mL
-
Proveta de 100 mL

-
Água (50 mL)
-
1 colher de chá de cloreto de sódio (sal de cozinha)
-
Gasolina (50 mL)
c) Passo a passo para determinar o teor de álcool na gasolina
1o Passo:
Adicionar todo o cloreto de sódio no béquer.
2o Passo:
Adicionar a água aos poucos ao béquer que está com o cloreto de sódio e misturar até que o volume final de água adicionado seja de 50 mL.
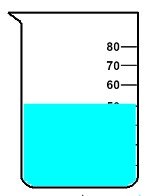
Béquer com a mistura de água e cloreto de sódio
3o Passo:
Adicionar toda a gasolina (50 mL) no interior da proveta.

Representação da gasolina na proveta
4o Passo:
Adicionar toda a mistura de água com cloreto de sódio no interior da proveta.
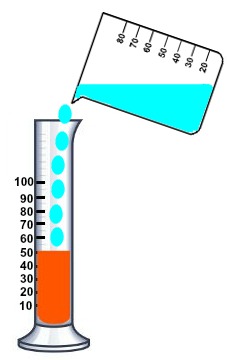
Adição da mistura (água e cloreto de sódio) na gasolina
5o Passo:
Tampar a proveta e agitar a mistura.
6o Passo:
Aguardar cerca de 15 minutos.
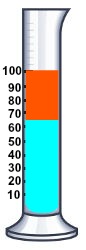
Representação do conteúdo da proveta após o tempo de espera
d) Discussão e explicação do experimento
A água é uma substância polar, assim como o sal de cozinha (cloreto de sódio). Por isso, quando misturamos os dois, o sal dissolve-se na água e forma uma mistura homogênea e bastante polarizada.
A gasolina, por sua vez, é uma substância apolar, e o etanol apresenta uma parte de sua molécula apolar e outra polar. Por esse motivo, o álcool dissolve-se na gasolina. Assim, a mistura gasolina e etanol também é homogênea.
Quando colocamos no mesmo recipiente as duas misturas homogêneas, o etanol, que apresenta uma região polar em sua molécula, automaticamente passa a interagir com a mistura de água e cloreto de sódio, dissolvendo-se nela. Com isso, a gasolina é separada do etanol.
Com o tempo, a gasolina desloca-se para cima da mistura de água, cloreto de sódio e etanol por ser menos densa.
e) Determinação do teor de álcool na gasolina
As quantidades utilizadas no experimento foram:
-
Gasolina (com etanol) = 50 mL
-
Mistura água e cloreto de sódio = 50 mL
Quantidade ao final do experimento:
-
Gasolina= 35 mL (já que sua medida começa na marca de 65 mL e vai até 100 mL)
-
Mistura água, etanol e cloreto de sódio = 65 mL
Como tínhamos no início 50 mL de gasolina e, ao final, apenas 35 mL, concluímos que havia 15 mL de etanol dissolvidos na gasolina.
Para calcularmos a porcentagem de etanol que estava presente na gasolina, basta montar a seguinte regra de três:
50 mL de gasolina inicial ---------- 100%
15 mL de etanol presentes -------- x
50.x = 15.100
50x = 1500
x = 1500
50
x = 30%
Como o limite de etanol permitido é de 27%, o combustível desse experimento estaria adulterado.
Por Me. Diogo Lopes Dias
Videoaula relacionada: