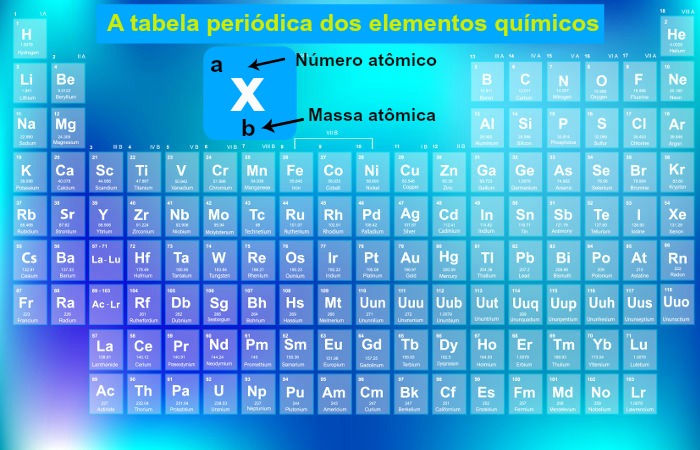
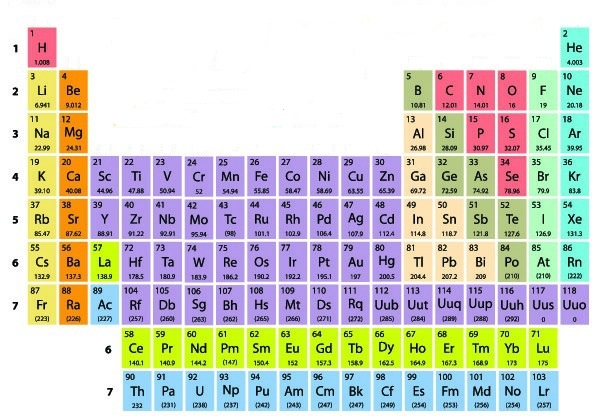
Famílias da tabela periódica
As famílias da tabela periódica correspondem às 18 colunas presentes nessa ferramenta. Também chamadas de grupos, elas agrupam elementos químicos com propriedades semelhantes.
Por Stéfano Araújo Novais
PUBLICIDADE
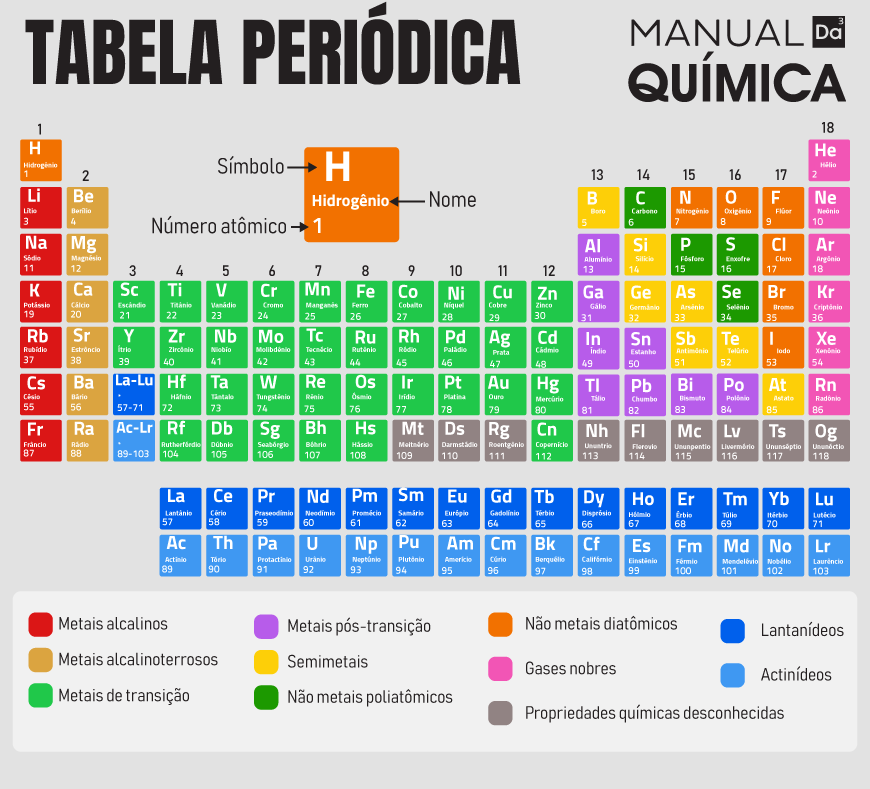
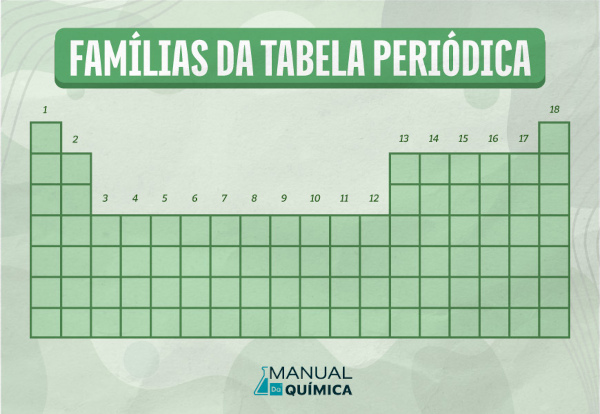
As famílias da tabela periódica (também chamadas de grupos) consistem nas 18 colunas que constituem essa ferramenta. A partir de 1988, ficou acordado que as famílias seriam sinalizadas por números, do 1 até o 18, iniciando nos metais alcalinos e encerrando nos gases nobres.
As famílias da tabela periódica agrupam elementos de propriedades físicas e químicas semelhantes e de mesma configuração de camada de valência. Além disso, a avaliação dessas famílias é essencial para o entendimento das propriedades periódicas. As famílias também são usadas para determinar quais são os elementos representativos e os elementos de transição da tabela periódica.
Leia também: Quantos elementos existem na tabela periódica?
Resumo sobre famílias da tabela periódica
- As famílias da tabela periódica são as colunas que estão presentes nessa ferramenta.
- Ao todo, a tabela periódica é composta por 18 famílias, as quais são numeradas, desde 1988, de 1 até 18.
- As famílias agrupam elementos com propriedades físicas e químicas semelhantes.
- Algumas famílias possuem nomes históricos, como é o caso dos metais alcalinos (família 1) e dos gases nobres (família 18).
- As famílias da tabela periódica são importantes na divisão dos elementos em representativos e de transição, além de análise de propriedades periódicas.
O que são as famílias da tabela periódica?
As famílias (ou grupos) da tabela periódica consistem nas 18 colunas que a constituem. Desde 1988, as famílias são numeradas de 1 a 18, não usando mais a numeração com A e B. O nome “família”, embora ainda muito comum, não é mais recomendado, dando lugar ao termo “grupo”.
Nome das famílias da tabela periódica
Algumas famílias da tabela periódica recebem nomes históricos, conforme tabela a seguir:
|
Família |
Nome |
|
1 |
metais alcalinos (exceção do hidrogênio) |
|
2 |
metais alcalino-terrosos |
|
16 |
calcogênios |
|
17 |
halogênios |
|
18 |
gases nobres |
Alguns autores também citam a família 15, do nitrogênio, como pnictogênios (ou pinictogênios). As demais famílias, as quais não levam nomes históricos, podem ser identificados pelo número ou pelo elemento que as inicia. Por exemplo, a família 8 pode ser também chamada de família do ferro.
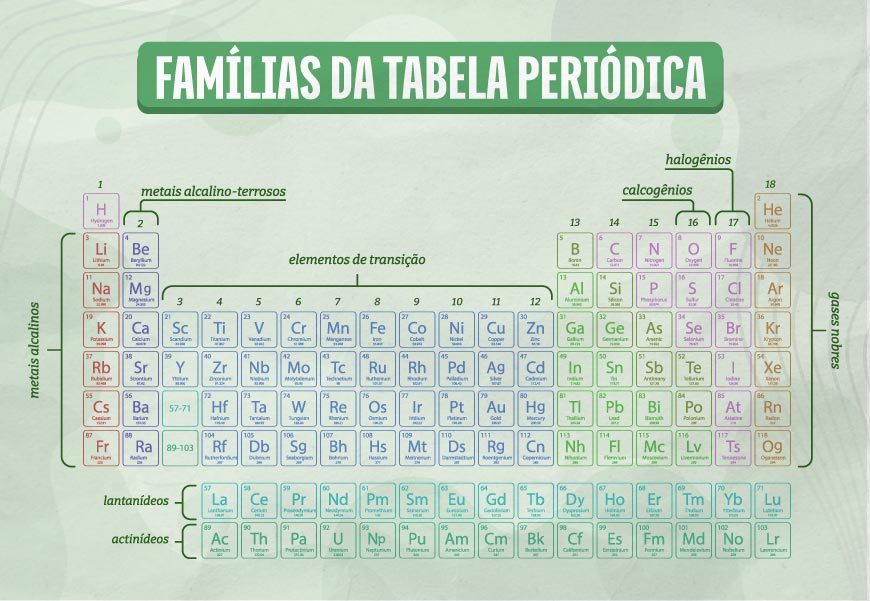
Características das famílias da tabela periódica
As famílias da tabela periódica são numeradas de 1 até 18, iniciando com os metais alcalinos e finalizando nos gases nobres. Nas famílias, estão alocados os elementos com propriedades químicas e físicas semelhantes. Outro ponto importante, mais ligado à estrutura atômica, é que elementos químicos da mesma família apresentam a mesma configuração da camada de valência.
A avaliação das famílias também é importante para entendimento das propriedades periódicas. O raio atômico aumenta, na família, no sentido de cima para baixo. Já a energia de ionização, a afinidade eletrônica e a eletronegatividade aumentam no sentido de baixo para cima na família.
Veja também: Quais são os períodos da tabela periódica?
Elementos representativos
As famílias são usadas para determinar quais são os elementos representativos. São considerados como elementos representativos os elementos alocados nas famílias 1, 2 e também nas famílias 13 até 18.
Elementos de transição
As famílias de 3 a 12 apresentam os elementos de transição. Alguns autores não reconhecem os elementos da família 12 como elementos de transição, pois entende-se que, para ser de transição, eles devem possuir subnível d incompleto ou gerar cátions com subnível d incompleto. Isso não ocorre com os elementos do grupo 12.
Dentro dos elementos de transição, no grupo 3, estão os lantanídeos e actinídeos. Esses elementos são conhecidos como elementos de transição interna. Dessa forma, os demais elementos são conhecidos como elementos de transição externa.
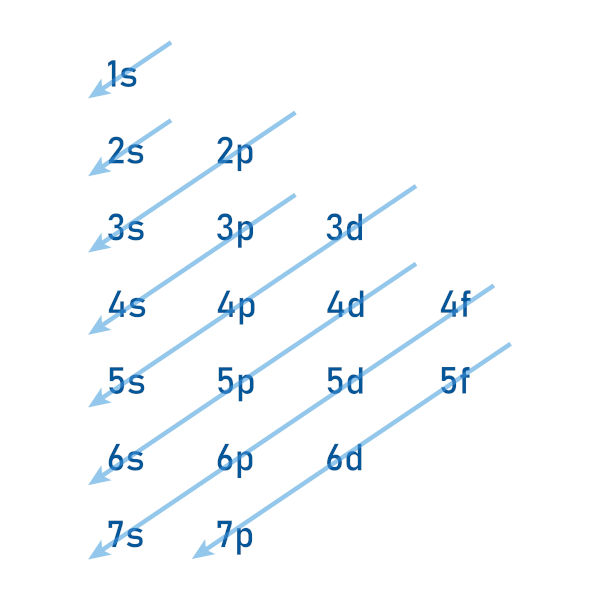
Tabela periódica e distribuição eletrônica
A tabela periódica pode ser útil para determinar a configuração eletrônica dos elementos. No caso, dentro da tabela podemos dividir algumas famílias quanto ao seu subnível da camada de valência.
Assim, temos:
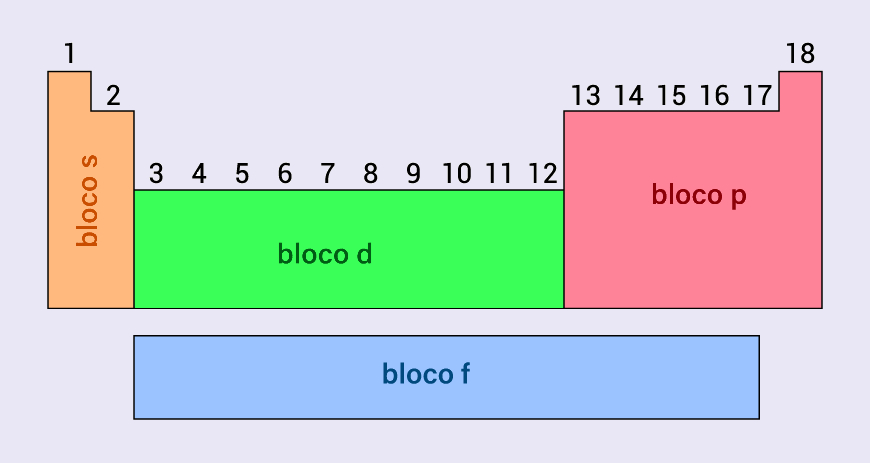
- Famílias 1 e 2: bloco s
- Famílias 3 até 12: bloco d
- Famílias 13 até 18: bloco p
- Lantanídeos e actinídeos: bloco f
- Elementos do bloco s: apresentarão a configuração eletrônica [GN] nsx, onde “[GN]” é o símbolo do gás nobre imediatamente anterior, “n” é o período que se encontra o elemento e “x” poderá ser igual a 1 ou 2, sendo 1 para a família 1 e 2 para a família 2. Por exemplo, para o sódio, que está na família 1, terceiro período, a sua distribuição é [Ne] 3s1.
- Elementos do bloco p: apresentarão distribuição eletrônica do tipo [GN] ns2 npx. Nesse caso, o valor de x pode variar de 1 (para elementos da família 13) até 6 (para elementos da família 18). Por exemplo, o oxigênio, que está na família 16, segundo período, apresenta uma distribuição eletrônica [He] 2s2 2p4.
- Elementos do bloco d: apresentarão a configuração eletrônica como [GN] ns2 (n-1)dx. Agora, x pode variar de 1 (para elementos da família 3) até 10 (para elementos da família 12). Por exemplo, o ferro, que está na família 8, quarto período, apresenta a distribuição eletrônica [Ar] 4s2 3d6.
- Elementos do bloco f: apresentarão uma configuração eletrônica que pode ser entendida como [GN] ns2 (n-2)fx. Agora, o valor de x pode estar entre 1 e 14. Um exemplo é o samário, lantanídeo de número atômico 62, cuja configuração eletrônica é [Xe] 6s2 4f6.
Saiba mais: Eletronegatividade x eletropositividade — qual a diferença?
Exercícios resolvidos sobre famílias da tabela periódica
Questão 1. (USS-Univassouras – Medicina/2025.2) Um metal empregado em próteses ortopédicas corresponde ao elemento químico de maior energia de ionização situado no grupo 4 da tabela de classificação periódica.
O símbolo desse elemento químico é:
A) Zr.
B) Ti.
C) Rf.
D) Hf.
Resposta: Letra B.
Nos grupos (ou famílias), a energia de ionização cresce no sentido de baixo para cima, ou seja, em uma mesma família quanto menor o período do elemento, maior sua energia de ionização. Dessa forma, para o grupo 4, o elemento de maior energia de ionização é o titânio (Ti).
Questão 2. (UECE – 1ª fase/2025.2) A água mineral é formada no momento em que as águas das chuvas penetram no solo e vão atravessando diversas camadas até chegar às camadas impermeáveis, onde estacionam. Nesse trajeto por baixo do solo, a água passa por várias rochas cheias de substâncias minerais, como o carbonato e o sulfato de cálcio, que se diluem na água, enriquecendo-a e fazendo com que ela adquira propriedades medicinais valiosas. Existem sais minerais presentes na água mineral, dentre eles, os sais de cálcio, potássio, magnésio e sódio.
Com relação a esses minerais, sejam as duas afirmativas a seguir:
( ) sódio e potássio são metais alcalinos e, na classificação periódica, estão no mesmo período.
( ) magnésio e cálcio são metais alcalinos terrosos e, na classificação periódica, estão em períodos diferentes.
Marcando com V a afirmativa verdadeira e com F a afirmativa falsa, assinale a sequência correta de cima para baixo.
A) F, F.
B) F, V.
C) V, F.
D) V, V.
Resposta: Letra B.
A primeira afirmativa é falsa, uma vez que os metais alcalinos ficam, na verdade, na mesma família (coluna) e não no mesmo período.
Fontes
ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de Química: Questionando a vida e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018.
SANTOS, Lucas Henrique Ferreira dos; ALMEIDA, José de Arimateia da Silva. Uma Proposta para a Abordagem da Tabela Periódica nos Cursos de Formação de Professores de Ciências e no Ensino Médio a partir do Tema Metais. Revista Virtual de Química, [Niterói], v. 13, n. 3, p. 741-754, 2021. Disponível em: https://scispace.com/pdf/a-proposal-for-the-periodic-table-teaching-in-science-3qw5ktsgid.pdf.